
| 成分 | 质量(g) | 摩尔质量(g/mol) |
| 蔗糖(C12H22O11) | 25.00 | 342 |
| 硫酸钾(K2SO4) | 0.25 | 174 |
| 高锰酸钾(KMnO4) | 0.25 | 158 |
| 阿司匹林(C9H8O4) | 0.17 | 180 |
| 硝酸银(AgNO3) | 0.02 | 170 |
分析 (1)电解质知在溶液中或熔融状态下能导电的化合物,据此分析;
(2)根据溶液的配制步骤来分析使用的仪器;
(3)K+来自高锰酸钾、硫酸钾的电离,由n=$\frac{m}{M}$计算高锰酸钾、硫酸钾的物质的量,根据钾离子守恒可知n(K+)=n(KMnO4)+2n(K2SO4),再根据物质的量浓度定义计算钾离子物质的量浓度.
解答 解:(1)a、蔗糖为非电解质,故A错误;
b、硫酸钾在水溶液中和熔融状态下均能导电,故为电解质,故b正确;
c、硝酸银在水溶液中和熔融状态下均能导电,故为电解质,故c正确;
故选bc.
(2)根据配制操作可知,因配制500mL溶液,则需选用500mL容量瓶,最后需胶头滴管定容,所以所需仪器除托盘天平、烧杯、玻璃棒、药匙外还需500mL容量瓶、胶头滴管.
故答案为:500mL容量瓶;
(3)高锰酸钾的物质的量为n(KMnO4)=$\frac{m}{M}$=$\frac{0.25g}{158g/mol}$=0.00158mol.
硫酸钾的物质的量为n(K2SO4)=$\frac{0.25g}{174g/mol}$=0.00143mol,
n(K+)=n(KMnO4)+2n(K2SO4)=0.00158mol+2×0.00143mol,
所以c(K+)=$\frac{0.00158mol+2×0.00143mol}{0.5L}$.
故答案为:$\frac{0.00158mol+2×0.00143mol}{0.5L}$.
点评 以鲜花保鲜剂为载体,主要考查溶液配制,难度中等,注意从c=$\frac{n}{V}$理解配制原理.


科目:高中化学 来源: 题型:选择题
| A.商代后母戊鼎 | B.新石器时代人面鱼纹彩陶盆 | C.明永乐青花竹石芭蕉纹梅瓶 | D.三国青瓷羊形烛台 |
 |  |  |  |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
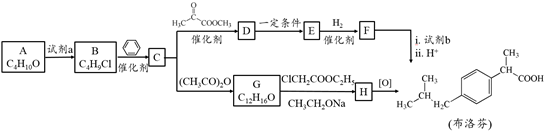

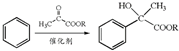
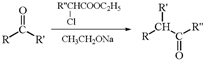
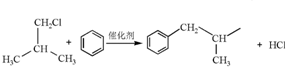 .
.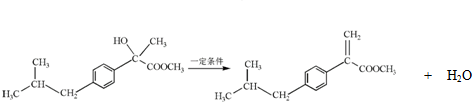 .
. ,H的含氧官能团的名称是醛基.
,H的含氧官能团的名称是醛基.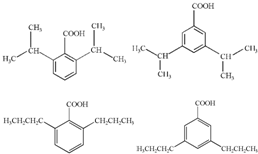 (其中两种).
(其中两种).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
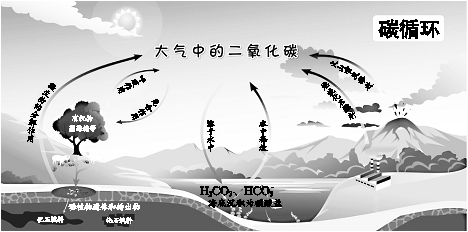
| A. | 呼吸作用涉及氧化还原反应 | B. | 碳循环具有全球性 | ||
| C. | 含碳化合物可相互转化 | D. | 碳元素均被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验事实 | 结论 |
| A | H2可在Cl2中燃烧 | 燃烧不一定有氧气参加 |
| B | 铝箔在酒精灯火焰上加热熔化但不滴落 | 氧化铝熔点高于铝 |
| C | 钠块投入水中,迅速熔成银白色小球 | 钠的密度比水小 |
| D | 某溶液中加入NaOH溶液,加热,产生使湿润红色石蕊试纸变蓝的气体 | 原溶液中含NH4+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
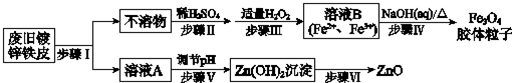
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向沸水中滴加FeCl3饱和溶液制备Fe(OH)3胶体:Fe3++3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3↓+3H+ | |
| B. | 向盐酸中滴加氨水:H++OH-═H2O | |
| C. | 金属钠与水反应:2Na+2H2O═2Na++2OH-+H2↑ | |
| D. | 用FeCl3溶液腐蚀印刷电路铜板:Fe3++Cu═Fe2++Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com