
ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ
A£®ÓŠ»śĪļCH2=CH-CH3ÖŠĢ¼µÄŌÓ»ÆĄąŠĶÓŠsp3 ŗĶsp2£¬ĘäÖŠÓŠĮ½øö¦Š¼ü£¬7øö¦Ņ¼ü
B£®·Ö×ÓCOŗĶN2µÄŌ×Ó×ÜŹżĻąĶ¬£¬¼Ūµē×Ó×ÜŹżĻąµČ
C£®Na+µÄµē×ÓÅŲ¼Ź½ĪŖ1s22s22p6
D£®CO2·Ö×ӵĹ¹ŠĶĪŖÖ±ĻߊĶ
 ĆūŠ£æĪĢĆĻµĮŠ“š°ø
ĆūŠ£æĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğŗž±±Ź”»ĘŹÆŹŠø߶žĻĀŃ§ĘŚĘŚÖŠæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠÓŠ¹ŲŹż¾ŻµÄ±Č½Ļ£¬²»ÕżČ·µÄŹĒ( )
A£®ŌŖĖŲµÄ¼Ūµē×ÓŹżŗĶĖłŌŚ×åµÄ×åŠņŹżĻąµČ
B£®NaOH¾§ĢåÖŠµÄŃōĄė×ÓŗĶŅõĄė×ÓŹżÄæĻąµČ
C£®CsCl¾§ĢåÖŠĆæøöCs£«ÖÜĪ§½ōĮŚµÄCl£ŗĶĆæøöCl£ÖÜĪ§½ōĮŚµÄCs£«øöŹżĻąµČ
D£®[Co(NH3)6]3£«ÖŠµÄNH3·Ö×ÓŹżÓėÅäĪ»¼üŹżĻąµČ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğŗÓÄĻŹ”ÖÜæŚŹŠø߶žĻĀŃ§ĘŚĘŚÖŠæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠÓŠ»śĪļĆüĆūÕżČ·µÄŹĒ
A£®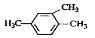 1£¬3£¬4-Čż¼×±½ B£®
1£¬3£¬4-Čż¼×±½ B£®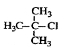 2-¼×»ł-2-ĀȱūĶé
2-¼×»ł-2-ĀȱūĶé
C£®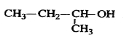 2-¼×»ł-1-±ū“¼ D£®
2-¼×»ł-1-±ū“¼ D£®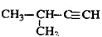 2-¼×»ł-3-¶”Č²
2-¼×»ł-3-¶”Č²
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģɽĪ÷Ź”øßČżµŚ¶žĀÖѵĮ·Īå»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
Ņ»ĀČ“śĢžA(C5H11Cl)¾Ė®½āŗóŌŁŃõ»ÆæɵƵ½ÓŠ»śĪļB£¬AµÄŅ»ÖÖĶ¬ĻµĪļ(C4H9Cl)¾Ė®½āµĆµ½ÓŠ»śĪļC£¬B ŗĶCæÉ·¢Éśõ„»Æ·“Ӧɜ³Éõ„D£¬ŌņDæÉÄܵĽį¹¹ÓŠ( )ÖÖ
A£®12 B£®16 C£®24 D£®32
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğ¹ć¶«ÉĒĶ·½šÉ½ÖŠŃ§ø߶žĻĀµŚŹ®¶žÖÜĮ·»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
ĻĀ±ķŹĒŌŖĖŲÖÜĘŚ±ķµÄŅ»²æ·Ö”£±ķÖŠĖłĮŠµÄ×ÖÄø·Ö±š“ś±ķŅ»ÖÖ»ÆѧŌŖĖŲ”£
a | b | ||||||||||||||||
c | d | e | |||||||||||||||
f | g | ||||||||||||||||
ŹŌ»Ų“šĻĀĮŠĪŹĢā£Ø·²Éę¼°µÄĪļÖŹ¾łÓĆ»ÆѧŹ½±ķŹ¾£©£ŗ
£Ø1£©aµÄĒā»ÆĪļµÄ·Ö×Ó¹¹ŠĶĪŖ £¬ÖŠŠÄŌ×ÓµÄŌӻƊĪŹ½ĪŖ £»dµÄ×īøß¼ŪŃõ»ÆĪļµÄ·Ö×Ó¹¹ŠĶĪŖ £¬ÖŠŠÄŌ×ÓµÄŌӻƊĪŹ½ĪŖ £¬øĆ·Ö×ÓŹĒ £ØĢī”°¼«ŠŌ”±»ņ”°·Ē¼«ŠŌ”±£©·Ö×Ó”£
£Ø2£©b”¢d”¢eČżÖÖŌŖĖŲµÄĒā»ÆĪļÖŠµÄ·Šµć×īøߵďĒ £¬ŌŅņŹĒ£ŗ ”£
£Ø3£©½«gµÄĪŽĖ®ĮņĖįŃĪČܽāÓŚĖ®ÖŠ£¬ČÜŅŗ³ŹĄ¶É«£¬ŹĒŅņĪŖÉś³ÉĮĖŅ»ÖÖ³ŹĄ¶É«µÄÅäŗĻĄė×Ó£¬Š“³öøĆÅäŗĻĄė×ӵĽį¹¹¼ņŹ½(±ŲŠė½«ÅäĪ»¼ü±ķŹ¾³öĄ“) ”£
£Ø4£©f (NH3)5BrSO4æÉŠĪ³ÉĮ½ÖÖÅäŗĻĪļ £¬ŅŃÖŖf 3£« µÄÅäĪ»ŹżŹĒ6£¬ĪŖČ·¶ØfµÄÅäŗĻĪļµÄ½į¹¹£¬ĻÖ¶ŌĮ½ÖÖÅäŗĻĪļ½ųŠŠČēĻĀŹµŃé£ŗŌŚµŚŅ»ÖÖÅäŗĻĪļµÄČÜŅŗÖŠ¼ÓBaCl2 ČÜŅŗŹ±£¬²śÉś°×É«³Įµķ£¬ŌŚµŚ¶žÖÖÅäŗĻĪļČÜŅŗÖŠ¼ÓČėBaCl2ČÜŅŗŹ±£¬ŌņĪŽĆ÷ĻŌĻÖĻ󣬵Ś¶žÖÖÅäŗĻĪļµÄ»ÆѧŹ½ĪŖ £¬øĆÅäŗĻĪļµÄÅäĢåŹĒ ”¢ £»
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğ¹ć¶«ÉĒĶ·½šÉ½ÖŠŃ§ø߶žĻĀµŚŹ®¶žÖÜĮ·»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŅŃÖŖŗ¬ŃõĖįæÉÓĆĶØŹ½XOn£ØOH£©mĄ“±ķŹ¾£¬ČēXŹĒS£¬Ōņm=2£¬n=2£¬ŌņÕāøöŹ½×Ó¾Ķ±ķŹ¾H2SO4”£Ņ»°ć¶ųŃŌ£¬øĆŹ½ÖŠn“óµÄŹĒĒæĖį£¬nŠ”µÄŹĒČõĖį”£ĻĀĮŠø÷ŗ¬ŃõĖįÖŠĖįŠŌ×īĒæµÄŹĒ
A£®H2SeO3 B£®HMnO4 C£®H3BO3 D£®H3PO4
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğ¹ć¶«ÉĒĶ·½šÉ½ÖŠŃ§ø߶žĻĀµŚŹ®¶žÖÜĮ·»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®±łČŪ»ÆŹ±£¬·Ö×ÓÖŠH£O¼ü·¢Éś¶ĻĮŃ
B£®Ėę×ÅĀ±ĖŲŌ×Óµē×Ó²ćŹżµÄŌö¼Ó£¬Ā±»ÆĪļCX4·Ö×Ó¼ä×÷ÓĆĮ¦Öš½„Ōö“ó£¬ĖłŅŌĖüĆĒĻąÓ¦µÄČŪ·ŠµćŅ²Öš½„Ōöøß
C£®ÓÉÓŚH”ŖO¼ü±ČH”ŖS¼üĄĪ¹Ģ£¬ĖłŅŌĖ®µÄČŪ·Šµć±ČH2Søß
D£®ŌŚÓÉ·Ö×ÓĖł¹¹³ÉµÄĪļÖŹÖŠ£¬·Ö×Ó¼ä×÷ÓĆĮ¦Ō½“ó£¬øĆĪļÖŹŌ½ĪȶØ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğ°²»Õ»ĘɽĶĶĻŖŅ»ÖŠøßŅ»ĻĀĘŚÖŠ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠø÷×éµÄµē¼«²ÄĮĻŗĶµē½āŅŗ£¬²»ÄÜ×é³ÉŌµē³ŲµÄŹĒ
A£®Ķʬ”¢Ķʬ”¢Ļ”ĮņĖį B£®Ķʬ”¢ŹÆÄ«°ō”¢ĻõĖįŅųČÜŅŗ
C£®Šæʬ”¢Ķʬ”¢Ļ”ĮņĖį D£®Ķʬ”¢Ņųʬ”¢FeCl3ČÜŅŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģĪ÷²ŲČÕæ¦ŌņŅ»ÖŠøßČżĻĀѧʌ¶žÄ£æ¼ŹŌĄķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
µŚČżÖÜĘŚŌŖĖŲR£¬ĖüµÄŌ×Ó×īĶāµē×Ó²ć“ļµ½ĪČ¶Ø½į¹¹ĖłĖłŠčµÄµē×ÓŹżÉŁÓŚ“ĪĶā²ćÓė×īÄŚ²ćµē×ÓŹżÖ®²ī£¬ĒŅµČÓŚ×īÄŚ²ćµē×ÓŹżµÄÕūŹż±¶£¬¹ŲÓŚRµÄŠšŹöÖŠÕżČ·µÄŹĒ( )
A£®³£ĪĀĻĀ£¬ÄÜĪČ¶Ø“ęŌŚµÄRµÄŃõ»ÆĪļ¶¼ŹĒĖįŠŌŃõ»ÆĪļ
B£®RµÄĘųĢ¬Ēā»ÆĪļµÄĖ®ČÜŅŗ¾ßÓŠĒæĖįŠŌ
C£®RŹĒ½šŹōŌŖĖŲ
D£®RµÄĘųĢ¬Ńõ»ÆĪļ²»ÄÜŌŚŃõĘųÖŠČ¼ÉÕ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com