
下列说法正确的是
A.分子内共价键越强,分子越稳定,其熔沸点也越高
B.C、H、O、N四种元素组成的化合物一定是离子化合物
C.HF分子间存在着氢键,所以HF比HCl稳定
D.由原子构成的晶体可能是原子晶体,也可能是分子晶体
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016届黑龙江省高三上学期12月月考化学试卷(解析版) 题型:选择题
下列排列顺序正确的是( )
①热稳定性:H2O>HF>H2S ②原子半径:Na>Mg>O ③沸点:H2Se>H2S>H2O
④结合H+能力:OH->CH3COO->I-
A.①③ B.②③ C.①④ D.②④
查看答案和解析>>
科目:高中化学 来源:2016届辽宁省大连市高三上12月月考理综化学试卷(解析版) 题型:实验题
资料显示:a.Na2S2O3、BaS2O3、BaS均易溶于水。b.SO2、Na2S、Na2CO3反应可生成Na2S2O3。
某化学小组据此进行了制备硫代硫酸钠(Na2S2O3)的探究:
实验制备装置如下图所示(省略夹持装置):
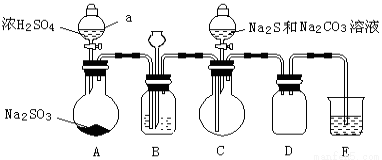
回答问题:
(1)仪器a的名称是 。
(2)装置B中的长颈漏斗的作用是
(3)在装置C中生成Na2S2O3。
①完成反应方程式: SO2 + Na2S + Na2CO3 = Na2S2O3 +
②反应开始先使A中发生反应一会儿,再使C中反应发生,其原因是 。
(4)完成对所得产品的检测的实验:
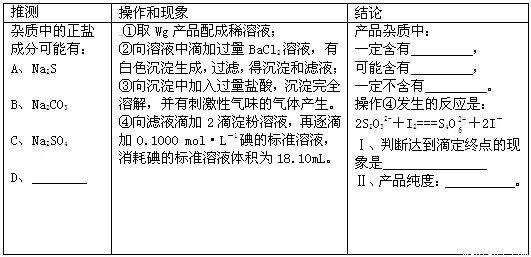
查看答案和解析>>
科目:高中化学 来源:2016届内蒙古赤峰二中高三上学期12月月考理综化学试卷(解析版) 题型:填空题
二甲醚(CH3OCH3)是一种重要的清洁燃料气,其储运、燃烧安全性、理论燃烧温度等性能指标均优于液化石油气,也可用作燃烧电池,具有很好的发展前景。
(1)已知H2、CO和CH3OCH3的燃烧热(ΔH)分别为-285.5kJ/mol、-283kJ/mol和-1460.0 kJ/mol,则工业上利用水煤气成分按1:1合成二甲醚的热化学方程式为:____________。
(2)工业上采用电浮远凝聚法处理污水时,保持污水的pH在5.0,通过电解生成Fe(OH)3胶体,吸附不溶性杂质,同时利用阴极产生的H2,将悬浮物带到水面,利于除去。实验室以二甲醚燃料电池模拟该方法设计的装置如下图所示:
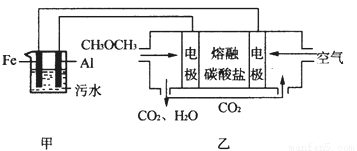
①乙装置以熔融碳酸盐为电解质,稀土金属材料为电极。写出该燃料电池的正极电极反应式 __________________;下列物质可用做电池熔融碳酸盐的是 ______。
A.MgCO3 B.Na2CO3 C.NaHCO3 D.(NH4)2CO3
②写出甲装置中阳极产物离子生成Fe(OH)3沉淀的离子方程式____________________ 。
③已知常温下Ksp[Fe(OH)3]=4.0×10-38,电解一段时间后,甲装置中c(Fe3+)= ___________。
④已知:H2S的电离平衡常数:K1=9.1×10-8、K2=1.1×10-12;H2CO3的电离平衡常数:K1=4.31×10-7、K2=5.61×10-11。测得电极上转移电子为0.24mol时,将乙装置中生成的CO2通入200mL 0.2mol/L的Na2S溶液中,下列选项正确的是______
A.发生反应的离子方程式为:CO2+S2-+H2O=CO32-+H2S
B.发生反应的离子方程式为:CO2+S2-+H2O=HCO3-+HS-
C.c(Na+)=2[c(H2S)+c(HS-)+c(S2-)
D.c(Na+)+c(H+)=2c(CO32-)+2c(S2-)+c(OH-)
E.c(Na+)>c(HCO3-)>c(HS-)>c(OH-)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广西柳州铁路第一中学高二上段考理化学卷(解析版) 题型:选择题
下列反应中,属于水解反应且使溶液显酸性的是
A.NH3 +H2O  NH4+ +OH- B.HCO3- + H2O
NH4+ +OH- B.HCO3- + H2O  C
C O32- + H3O+
O32- + H3O+
C.S2- + H2O HS- + OH- D. NH4+ + H2O
HS- + OH- D. NH4+ + H2O NH3·H2O + H+
NH3·H2O + H+
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广西桂林中学高二上期中考试理化学试卷(解析版) 题型:推断题
下图中A、B、C、D、E、F、G、H均为有机化合物,转化关系如图所示:
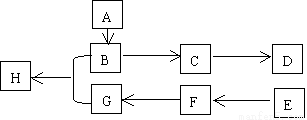
根据下面给出的信息回答问题:
(1)有机化合物A的相对分子质量小于60,A能发生银镜反应,1mol A在催化剂作用下能与3mol H2反应生成B,则A的结构简式是_________________,由A生成B的反应类型是__________________;
(2)B在浓硫酸中加热可生成C,C在催化剂作用下可聚合生成高分子化合物D,由C生成D的化学方程式是__________________________________________________________________;
(3)①芳香化合物E的分子式C8H8Cl2,E的苯环上的一溴取代物只有一种,则E可能结构简式是__________________________________________________________________(写两种)
②E在NaOH水溶液中可转变为F,F用高锰酸钾酸性溶液氧化生成G(C8H6O4)。1molG与足量的NaHCO3溶液反应可放出44.8LCO2(标准状况),由此确定E的结构简式是__________________;
(4)G和足量的B在浓硫酸催化作用下加热反应可生成H,则由G和B生成H的化学方程式是______________________________________________________,该反应的反应类型是 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东广州执信中学高一上期中考试化学试卷(解析版) 题型:填空题
居民饮用水的质量必须符合国家标准,以下是源水处理成自来水的工艺流程示意图。看图后回答下列问题。

(1)源水中含Ca2+、Mg2+、HCO3-、Cl? 等,加入过量石灰后生成Ca?OH?2,进而发生若干复分解反应,例如:HCO3-+OH-=CO32-+H2O 请写出另一个属于复分解反应的离子方程式 。
(2)凝聚剂除去悬浮固体颗粒的过程
①只是物理过程 ②只是化学过程 ③是物理和化学过程
FeSO4·7H2O是常用的凝聚剂,其在水中电离出的Fe2+离子被溶解在水中的O2所氧化为Fe3+,最终生成胶状沉淀,这种胶状沉淀是 (写化学式)。
(3)配平下列反应方程式,并标出电子转移方向和数目。
?Fe2++ ?O2 + ?H+== ?Fe3++ ?H2O
上述反应中,每转移8mol电子,标准状况下消耗O2的体积为___________L。
(4)通入二氧化碳的目的是 和 。
(5)Cl2的作用是 。
(6)Cl2是常用的强氧化剂,请你尝试写出一个合理的Cl2作为氧化剂的化学方程式。____________。
查看答案和解析>>
科目:高中化学 来源:2016届山西平遥中学等重点中学高三第三次练兵化学试卷(解析版) 题型:填空题
某氯化铁与氯化亚铁的混合物。现要测定其中铁元素的质量分数,实验按以下
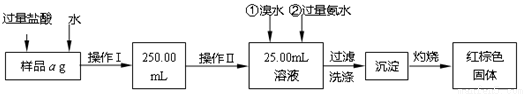
步骤进行:
Ⅰ.请根据上面流程,回答以下问题:
(1)操作Ⅰ所用的玻璃仪器除烧杯、玻璃棒外,还必须有 、 ,(填仪器名称)。
(2)请写出加入溴水发生的离子反应方程式 。
(3)将沉淀物加热,冷却至室温,用天平称量其质量为b1g,再次加热并冷却至室温称量其质量为b2g,若b1-b2=0.3g,则接下来还应进行的操作是 ;若蒸发皿质量是W1g,蒸发皿与加热后固体总质量是W2g,则样品中铁元素的质量分数是 。
Ⅱ.有同学提出,还可以采用以下方法来测定:
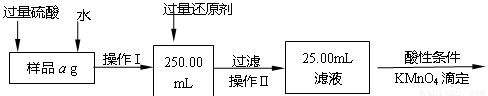
(1)溶解样品改用了硫酸,而不再用盐酸,为什么?
(2)选择的还原剂时否能用铁 (填“是”或“否”),原因是: 。
(3)若滴定用掉cmol/L高锰酸钾溶液bmL,则样品中铁元素的质量分数是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com