
| A. | Al(OH)3→Al2O3 | B. | Al2O3→Al(OH)3 | C. | Na2O2→NaOH | D. | Na2CO3→NaHCO3 |
分析 A.氢氧化铝分解生成氧化铝;
B.Al2O3与水不反应;
C.过氧化钠与水反应生成氢氧化钠;
D.碳酸钠溶液中通入过量的二氧化碳会生成碳酸氢钠.
解答 解:A.氢氧化铝分解生成氧化铝,所以Al(OH)3→Al2O3可以通过一步完成,故A不选;
B.Al2O3与水不反应,Al2O3→Al(OH)3不能一步实现,故B选;
C.过氧化钠与水反应生成氢氧化钠,Na2O2→NaOH能一步实现,故C不选;
D.碳酸钠溶液中通入过量的二氧化碳会生成碳酸氢钠,Na2CO3→NaHCO3能一步实现,故D不选;
故选B.
点评 本题主要考查了钠、铝及其化合物的化学性质的应用,主要考查一步反应转化件的分析判断,熟悉物质的性质是解答的关键,题目难度不大.


科目:高中化学 来源: 题型:解答题
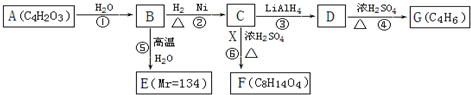
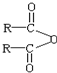 $\stackrel{H_{2}O}{→}$2RCOOH,RCOOH$\stackrel{LiAlH_{4}}{→}$RCH2OH
$\stackrel{H_{2}O}{→}$2RCOOH,RCOOH$\stackrel{LiAlH_{4}}{→}$RCH2OH ,1molA和足量的H2反应最多消耗掉H2的物质的量为1mol.
,1molA和足量的H2反应最多消耗掉H2的物质的量为1mol.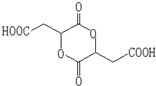 .
.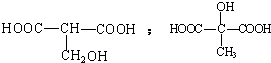 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
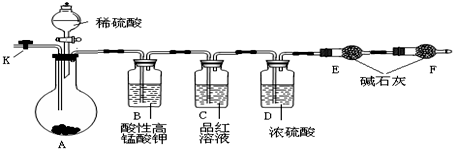
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 30g/mol | B. | 60g/mol | C. | 90g/mol | D. | 120g/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com