
对于:2H2(g) + O2(g) =2H2O(l) △H = —571.6kJ/mol的叙述错误的是
A.该反应的反应热为△H = —571.6kJ/mol ,是放热反应
B.该反应的△H与各物质的状态有关,与化学计量数也有关
C.该式的含义为:25℃、101 kPa下,2mol氢气完全燃烧生成液态水时放出热量571.6kJ
kPa下,2mol氢气完全燃烧生成液态水时放出热量571.6kJ
D.该反应为氢气燃烧的热化学方程式,由此可知氢气的燃烧热为571.6kJ/mol
 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案科目:高中化学 来源:2016届黑龙江省高三上12月月考化学试卷(解析版) 题型:选择题
下列说法不正确的是
A.Na与H2O的反应是熵增的放热反应,该反应能自发进行
B.饱和Na2SO4溶液或浓硝酸均可使蛋白质溶液产生沉淀,但原理不同
C.FeCl3和MnO2均可加快H2O2分解,同等条件下二者对H2O2分解速率的改变相同
D.Mg(OH)2固体在溶液中存在平衡:Mg(OH)2(s) Mg2+(aq)+2OH-(aq),该固体可溶于NH4Cl溶液
Mg2+(aq)+2OH-(aq),该固体可溶于NH4Cl溶液
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广西钦州港经济开发区中学高二上12月月考化学试卷(解析版) 题型:计算题
空气污染监测仪是根据二氧化硫与溴水的定量反应来测定空气中的二氧化硫含量的。
SO 2 +Br 2 +2H 2 O  2HBr+H 2 SO 4
2HBr+H 2 SO 4
上述反应的溴来自一个装有酸性(H 2 SO 4 )KBr溶液的电解槽阳极上的氧化反应。电解槽的阳极室与阴极室是隔开的。当测定某地区空气中SO 2 含量时,空气(已除尘)以1.5×10 -4 m 3·min -1 的流速进入电解槽的阳极室,电流计显示电子通过的速率是8.56×10 -11 mol·s -1 ,此条件下能保持溴浓度恒定并恰好与SO 2 完全反应(空气中不含能与溴反应的其他杂质)。写出上述材料中监测过程中发生的主要的化学反应方程式及该地区空气中SO 2 的含量(g·m -3 )。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高一上学期12月月考化学试卷(解析版) 题型:选择题
某溶液中Cl-、Br-、I- 三者物质的量之比为2︰3︰4,要使溶液中Cl-、Br-、I- 物质的量之比为1︰1︰1,则通入Cl2的物质的量是原溶液中I- 物质的量的
A.1/2 B.1/3 C.1/4 D.1/8
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高二上学期期中考试化学试卷(解析版) 题型:选择题
完全燃烧一定质量的无水乙醇,放出的热量为Q,已知为了完全吸收生成的二氧化碳气体,消耗掉8 mol/L的氢氧化钠溶液50 mL,则1 mol无水乙醇的燃烧放出的热量不可能是( )
A.10Q B.5Q~10Q C.3Q D.8Q
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高一上学期12月月考化学试卷(解析版) 题型:选择题
有两种金属组成的混合物粉末20g与足量的稀盐酸反应,生成22.4L(标准状况)H2,则该混合物的组成可能是
A.Fe 和Zn B.Al和Cu C.Na和Mg  D.Mg和Fe
D.Mg和Fe
查看答案和解析>>
科目:高中化学 来源:2016届福建省闽粤联合体高三上学期第三次联考化学试卷(解析版) 题型:实验题
实验室有一包固体粉末样品可能是MgCO3、Fe2O3和FeO的混合物。
I.甲学生设计实验方案,以确定样品中是否含有FeO。除样品外,实验室只提供以下试剂:KMnO4溶液、盐酸、稀硫酸、KSCN溶液、NaOH溶液,请你描述甲学生的实验操作步骤、现象及结论: 。
Ⅱ.经甲学生实验确定该样品中不存在FeO,乙学生想在甲学生的实验基础上进一步来测定混合物中Fe2O3的含量:乙学生准备用如图所示各仪器按一定顺序连接成一套完整的装置进行实验,以测定Fe2O3的质量分数。
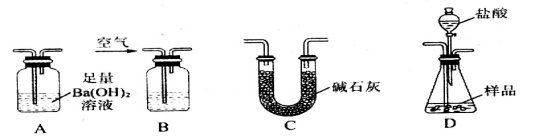
请回答下列问题:
(1)盛装盐酸的仪器的名称是 ,装置的连接顺序是:_____→_____→______→_____(填图中字母序号,各仪器只能选用一次)。
(2)实验过程中需要持续通入空气,其作用除可以起到“搅拌”A、D中反应物以实现充分反应外,还有一个重要作用是:____________________________。
(3)为提高测定的准确度,在B中最应加入的物质是: (填字母编号)。
a.饱和NaHCO3溶液 b.蒸馏水 c.浓硫酸 d.NaOH溶液
(4)在进行乙学生的实验方案评价时,有学生认为不必测定A中沉淀的质量,而只要测出装置A在吸收反应产生的气体前后的质量差,就能完成实验要求。实验证明,若用此法测得Fe2O3的质量分数将__________(填“偏大”、“偏小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源:2016届安徽省高三上1月阶段测理综化学试卷(解析版) 题型:实验题
阿司匹林(乙酰水杨酸, )是世界上应用最广泛的解热、镇痛和抗炎药.乙酰水杨酸受热易分解,分解温度为128~135℃.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下:
)是世界上应用最广泛的解热、镇痛和抗炎药.乙酰水杨酸受热易分解,分解温度为128~135℃.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下:
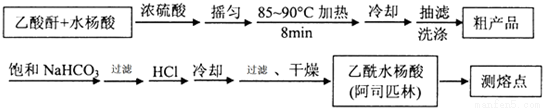
主要试剂和产品的物理常数
名称 | 相对分子质量 | 熔点或沸点(℃) | 水 |
水杨酸 | 138 | 158(熔点) | 微溶 |
醋酸 | 102 | 139.4(沸点) | 反应 |
乙酸水杨酸 | 180 | 135(熔点) | 微溶 |
请根据以上信息回答下列问题:
(1)制备阿司匹林时,要使用干燥的仪器的原因是_____________________;
(2)写出制备阿司匹林的化学方程式_____________________;
(3)①合成阿斯匹林时,最合适的加热方法是____________;
②过滤所得粗产品要用少量冰水洗涤,则洗涤的具体操作是_____________________;
(4)提纯粗产物中加入饱和NaHCO3溶液至没有CO2产生为止,再过滤,则加饱和NaHCO3溶液的目的是_____________________;另一种改进的提纯方法,称为重结晶提纯法.方法如下:
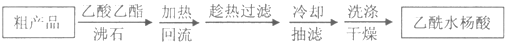
(5)改进的提纯方法中加热同流的装置如下图所示,使用温度计的目的是_______________;冷凝水的流进方向是__________(填“b”或“c”)。
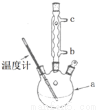
(6)检验产品中是否含有水杨酸的试剂是_______________;
(7)该学习小组在实验中原料用量:2.0g水杨酸、5.0mL醋酸酐(ρ=1.08g/cm3),最终称得产品m=2.2g,则所得乙酰水杨酸的产率为_______________;
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高一上第二次月考化学试卷(解析版) 题型:选择题
在5KCl+KClO3+3H2SO4=3Cl2↑+3K2SO4+3H2O中,被氧化的氯元素与被还原的氯元素的质量比为
A.1:1 B.5:1 C.1:5 D.3:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com