
| A. | 16 | B. | 14 | C. | 12 | D. | 28 |
 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源: 题型:解答题
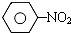 $\stackrel{Fe、HCl、H_{2}O}{→}$
$\stackrel{Fe、HCl、H_{2}O}{→}$
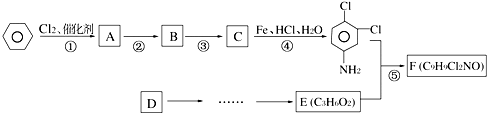
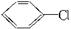 .反应②条件为浓硫酸加热.
.反应②条件为浓硫酸加热.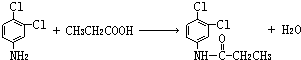 ;该反应的反应类型为取代反应.
;该反应的反应类型为取代反应.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 实验室欲配制980mL0.100mol•L-1Na2CO3溶液,需要用到下列仪器:烧杯、量筒、药匙、玻璃棒、托盘天平
实验室欲配制980mL0.100mol•L-1Na2CO3溶液,需要用到下列仪器:烧杯、量筒、药匙、玻璃棒、托盘天平查看答案和解析>>
科目:高中化学 来源: 题型:填空题
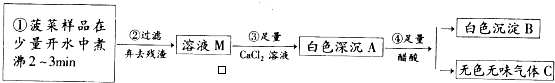
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | H2O(g)=H2(g)+$\frac{1}{2}$ O2(g)△H=+242 kJ/mol | B. | 2 H2(g)+O2(g)=2 H2O(g)△H=-484 kJ/mol | ||
| C. | H2(g)+$\frac{1}{2}$ O2(g)=H2O(g)△H=+242 kJ/mol | D. | 2 H2(g)+O2(g)=2 H2O(g)△H=+484 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
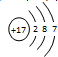 ,C的离子结构示意图
,C的离子结构示意图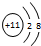 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
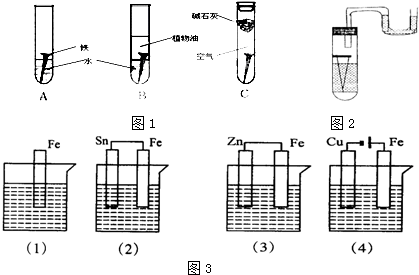
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
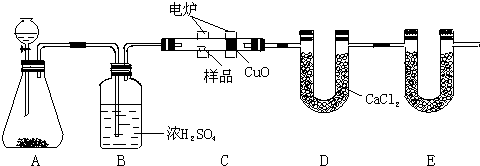
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com