
| A. | V(酸)=10V(碱) | B. | V(碱)=10V(酸) | C. | V(酸)=9V(碱) | D. | V(碱)=9V(酸) |
分析 100℃时,水的离子积Kw=10-12,某强酸溶液pH=4,则该酸溶液中氢离子浓度为10-4mol/L,强碱溶液pH=9,则碱溶液中氢氧根离子浓度=10-3 mol/L,混合后pH=6,说明氢离子和氢氧根离子的物质的量相等,据此计算酸溶液体积V酸和碱溶液体积V碱的关系.
解答 解:100℃时,水的离子积Kw=10-12,某强酸溶液pH=4,则该酸溶液中氢离子浓度为10-4mol/L,强碱溶液pH=9,则碱溶液中氢氧根离子浓度=10-3 mol/L,混合后pH=6,说明氢离子和氢氧根离子的物质的量相等,
则:10-4 mol/L×V(酸)=10-3 mol/L×V(碱),
整理可得:V(酸)=10V(碱),
故选A.
点评 本题考查了溶液酸碱性与溶液pH的计算,题目难度中等,根据溶液的酸碱性及水的离子积常数来分析解答,注意掌握溶液酸碱性与溶液pH的关系及计算方法.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
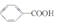 )和石灰的混合物得到一种液体,命名为苯.写出苯甲酸钠(
)和石灰的混合物得到一种液体,命名为苯.写出苯甲酸钠(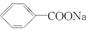 )与NaOH、生石灰共热生成苯的化学方程式:
)与NaOH、生石灰共热生成苯的化学方程式: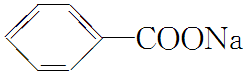 +NaOH
+NaOH  +Na2CO3.
+Na2CO3.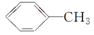 来制取
来制取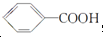 需要的试剂是KMnO4酸性溶液,下列物质属于苯的同系物且能被该试剂氧化的是d.
需要的试剂是KMnO4酸性溶液,下列物质属于苯的同系物且能被该试剂氧化的是d.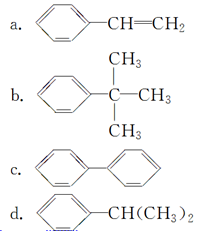
 .
.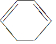 )脱去2mol氢原子变成苯却要放热,可推断苯比1,3-环己二烯稳定(填“稳定”或“不稳定”).
)脱去2mol氢原子变成苯却要放热,可推断苯比1,3-环己二烯稳定(填“稳定”或“不稳定”).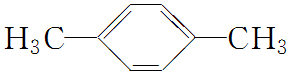 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
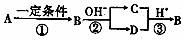 化合物A、B、C、D中均含有短周期元素X,B是一种常见的单质,它们有如图5所示的转化关系(部分产物与反应条件已略去),下列说法正确的是
化合物A、B、C、D中均含有短周期元素X,B是一种常见的单质,它们有如图5所示的转化关系(部分产物与反应条件已略去),下列说法正确的是| A. | X元素可能是金属,也可能是非金属 | |
| B. | 反应①、②、③均为氧化还原反应 | |
| C. | 反应②、③为可逆反应 | |
| D. | 若B为金属单质,反应①的“一定条件”为电解时,通常加入冰晶石作为助溶剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4NO3 | B. | NaOH | C. | MgSO4 | D. | Na2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(K+)+c(H+)═c(OH-)+c(HS-)+2 c(S2-) | B. | c(K+)>c(HS-)>c(OH-)>c(H+) | ||
| C. | c(HS-)+c(S2-)+c(H2S)=0.1 mol•L-1 | D. | c(K+)>c(HS-)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:W<X<Y<Z | |
| B. | 简单氢化物的稳定性:X>Y>Z | |
| C. | W分别与X、Z形成的化合物均能抑制水的电离 | |
| D. | 在化合物A 的分解反应中丙为氧化产物,丁为还原产物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com