
| A. | CuSO4只做还原剂 | |
| B. | 10mol CuSO4可氧化P的物质的量为2mol | |
| C. | Cu3P既是氧化产物,又是还原产物 | |
| D. | 生成1mol Cu3P时,被氧化的P的物质的量为2.2mol |
分析 P+CuSO4+H2O-Cu3P+H3PO4+H2SO4 反应中P元素的化合价由0升高为+5价,P元素的化合价由0降低为-3价,则P既是氧化剂又是还原剂,生成Cu3P为还原产物,H3PO4为氧化产物,Cu元素的化合价由+2价降低为+1价,则CuSO4为氧化剂,生成Cu3P为还原产物,以此来解答.
解答 解:A.Cu元素的化合价由+2价降低为+1价,则CuSO4为氧化剂,故A错误;
B.Cu元素的化合价由+2价降低为+1价,P元素的化合价由0升高为+5价,由得失电子守恒,则10mol CuSO4可氧化P的物质的量为$\frac{10×(2-1)}{5-0}$moL=2mol,故B正确;
C.根据以上分析,Cu3P仅为还原产物,故C错误;
D.由电子守恒可知,生成1mol Cu3P时,被氧化的P的物质的量为$\frac{1×3+1×(3-1)}{5-0}$mol=1.2mol,故D错误;
故选B.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念的考查,题目难度不大.


 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
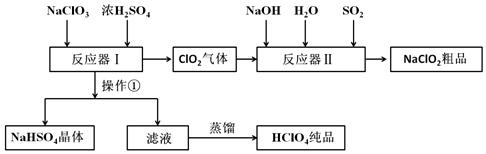
| 名称 | 分子式 | 外观 | 沸点 |
| 高氯酸 | HClO4 | 无色液体 | 130℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | amol-1 | B. | 2amol-1 | C. | 4amol-1 | D. | 8a mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com