
 氧元素和卤族元素都能形成多种物质,我们可以利用所学物质结构与性质的相关知识去认识和理解.
氧元素和卤族元素都能形成多种物质,我们可以利用所学物质结构与性质的相关知识去认识和理解.| 氟 | 氧 | 溴 | 碘 | |
| 第一电离能 (kJ/mol) | 1 681 | 1 251 | 1 140 | 1 008 |
分析 (1)COCl2中C原子的价电子对数为$\frac{4+2}{2}$=3,C原子采取sp2杂化,中心原子无孤电子对,C与O原子之间形成C=O双键,其结构式是 ,据此判断分子空间构型,溴是35号元素,最外层电子为其价电子,4s能级上排列2个电子,4p能级上排列5个电子,据此写出价电子排布式;
,据此判断分子空间构型,溴是35号元素,最外层电子为其价电子,4s能级上排列2个电子,4p能级上排列5个电子,据此写出价电子排布式;
(2)在离子晶体中离子半径越小,晶格能越大,据此判断;
(3)第一电离能是指原子失去一个电子所需的能量,第一电离能越小,就越容易失去一个电子,据此答题;
(4)A. HCl中存在s-pσ键,B.HF中存在s-pσ键,C. SO2中存在p-pπ键,D. SCl2中存在p-pσ键,据此答题;
(5)根据中心原子的价层电子对数确定其杂化方式;等电子体是具有相同的价电子数和相同原子数的微粒;
(6)根据均摊法确定晶胞中各种原子的个数,再确定其化学式,根据密度确定晶胞的体积,进而求得晶胞的边长,两个离得最近的钙是位于顶点和面心上的,它们的距离为晶胞边长的$\frac{\sqrt{2}}{2}$,据此答题;
解答 解:(1)COCl2中C原子的价电子对数为$\frac{4+2}{2}$=3,C原子采取sp2杂化,中心原子无孤电子对,C与O原子之间形成C=O双键,其结构式是 ,所以它的空间构型为平面三角形,溴是35号元素,最外层电子为其价电子,4s能级上排列2个电子,4p能级上排列5个电子,其价电子排布式为4s24p5,
,所以它的空间构型为平面三角形,溴是35号元素,最外层电子为其价电子,4s能级上排列2个电子,4p能级上排列5个电子,其价电子排布式为4s24p5,
故答案为:平面三角形;4s24p5;
(2)在离子晶体中离子半径越小,晶格能越大,比较两个反应的产物可知,由于氯离子的半径小于碘离子,所以CsCl的晶格能大于CsI的晶格能,故答案选A;
(3)第一电离能是指原子失去一个电子所需的能量,第一电离能越小,就越容易失去一个电子,比较表格中的数据可知,碘更容易形成较稳定的单核阳离子,
故答案为:碘;
(4)A. HCl中存在s-pσ键,B.HF中存在s-pσ键,C. SO2中存在p-pπ键,D. SCl2中存在p-pσ键,
故答案为:D;
(5)因为氯原子周围有四对价层电子,所以中心原子的杂化方式为sp3杂化;CN-中有两个原子,价电子数为10个,根据等电子体是具有相同的价电子数和相同原子数的微粒可知,它的等电子体分子是N2或 CO,
故答案为:sp3杂化;N2或 CO;
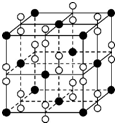
(6)根据均摊法可知晶胞中钙离子的个数为6×$\frac{1}{2}+8×$$\frac{1}{8}$=4,过氧离子的个数为12×$\frac{1}{4}$+1=4,故其化学式为CaO2,设晶胞的边长为a,根据ρ=$\frac{\frac{4×(40+32)}{{N}_{A}}}{a{\;}^{3}}$,得a=$\root{3}{\frac{72×4}{ρN{\;}_{A}}}$cm,两个离得最近的钙是位于顶点和面心上的,它们的距离为晶胞边长的 $\frac{\sqrt{2}}{2}$倍,即为$\frac{\sqrt{2}}{2}$×$\root{3}{\frac{72×4}{ρN{\;}_{A}}}$cm,
故答案为:CaO2;$\frac{\sqrt{2}}{2}$×$\root{3}{\frac{72×4}{ρN{\;}_{A}}}$.
点评 本题主要考查原子核外电子排布、晶格能、原子杂化轨道、晶胞的计算等知识点,中等难度,解题时注意基础知识的灵活运用.


 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案科目:高中化学 来源: 题型:填空题
| 化学键 | H-H | C-O | C≡O | H-O | C-H |
| E/(kJ•mol-1) | 436 | 343 | 1076 | 465 | 413 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
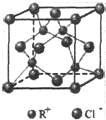 RCl常用作有机合成催化剂,并用于颜料,防腐等工业.R+中所有电子正好充满K、L、M三个电子层,它与Cl-形成的晶体结构如图所示.R的元素符号是Cu,每个Cl-周围最近的Cl-有12个.
RCl常用作有机合成催化剂,并用于颜料,防腐等工业.R+中所有电子正好充满K、L、M三个电子层,它与Cl-形成的晶体结构如图所示.R的元素符号是Cu,每个Cl-周围最近的Cl-有12个.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 与铝反应生成大量氢气的溶液中:Mg2+、K+、HCO3-、NO3- | |
| B. | 0.1mol/L的NaNO3溶液中:K+、I-、Cl-、SO42- | |
| C. | 铁与稀硫酸反应后的溶液中:[Fe(CN)6]3-、NH4+、Cl-、NO3- | |
| D. | 空气中:SO2、NO、N2、NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
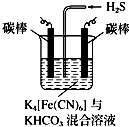 铁及其化合物在工农业生产、环境保护等领域中有着重要的作用.
铁及其化合物在工农业生产、环境保护等领域中有着重要的作用.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHCO3═Na++H++CO32- | B. | Na+2H2O═Na++2OH-+H2↑ | ||
| C. | 2Fe+6H+═Fe3++3H2↑ | D. | NaHSO4═Na++H++SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (CH3)2CHCH(CH3)OH | B. | (CH3CH2)2CHOH | C. | CH3CH2C(CH3)2OH | D. | CH3(CH2)3CH2OH |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com