
| A、pH=3的醋酸溶液中:c(H+)=c(CH3COO-)=3.0mol?L-1 |
| B、Na2S溶液中:c(Na+)>c(HS-)>c(OH-)>c(H2S) |
| C、pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| D、pH相同的①CH3COONa②NaHCO3③NaClO三种溶液的c(Na+):①>②>③ |


科目:高中化学 来源: 题型:
| A、铁和盐酸反应:Fe+2H+═Fe3++H2↑ |
| B、氢氧化钡溶液和稀硫酸反应:Ba2++SO42-═BaSO4↓ |
| C、氢氧化镁和盐酸反应:H++OH-═H2O |
| D、氣化铝溶液中加入过量氨水:Al3++3NH3?H2O═Al(OH)3↓+3NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、铜片上有气泡逸出 |
| B、溶液的pH逐渐减小 |
| C、电子由铜片经导线流向锌片 |
| D、该装置能将电能转化为化学能 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用广泛pH试纸测得某溶液的pH为6.3 |
| B、某常见气体的密度为1.8g?cm-3 |
| C、某澄清石灰水的浓度是2.0mol?L-1 |
| D、某元素的原子半径是111pm |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、HOCH2COOH的缩聚物是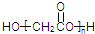 |
B、乙醛和丙烯醛(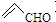 )不是同系物 )不是同系物 |
| C、已知甲醛分子中各原子共平面,则丙烯醛所有原子一定共平面 |
| D、结构为…-CH=CH-CH=CH-CH=CH-CH=CH-…的高分子的单体是1,3-丁二烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在自然界都以化合态存在 |
| B、易导电、易导热、有延展性 |
| C、金属元素原子的最外层电子数较少,易失去 |
| D、多数金属能被Cl2、S氧化,生成相应的氯化物或硫化物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com