
【题目】有四种不同堆积方式的金属晶体的晶胞如图所示,有关说法正确的是( )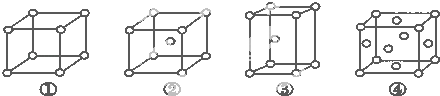
A.①为简单立方堆积②为六方最密堆积③为体心立方堆积④为面心立方最密堆积
B.每个晶胞含有的原子数分别为:①1个,②2个,③2个,④4个
C.晶胞中原子的配位数分别为:①6,②8,③8,④12
D.空间利用率的大小关系为:①<②<③<④
【答案】B
【解析】A.①为简单立方堆积、②为体心立方堆积,③为六方最密堆积、④为面心立方最密堆积,故A不符合题意;
B.①中原子个数=8× ![]() =1、②中原子个数=1+8×
=1、②中原子个数=1+8× ![]() =2、③中原子个数=1+8×
=2、③中原子个数=1+8× ![]() =2、④中原子个数=8×
=2、④中原子个数=8× ![]() +6×
+6× ![]() =4,故B符合题意;
=4,故B符合题意;
C.晶胞中原子的配位数分别为:①6,②8,③12,④中配位数=3×8× ![]() =12,故C不符合题意;
=12,故C不符合题意;
D.空间利用率:①52%、②68%、③74%、④74%,所以原子利用率顺序:①<②<③=④,故D不符合题意;
故答案为:B.
A.根据晶胞结构判断堆积方式;
B.根据均摊法进行计算晶胞含有的原子数;
C.根据晶胞结构和空间构型判断配位数;
D.根据各种堆积方式判断空间利用率的大小.


科目:高中化学 来源: 题型:
【题目】石油产品中除含有H2S外,还含有各种形态的有机硫,如COS、CH3SH等。
回答下列问题:
(1)CH3SH(甲硫醇)的电子式为__________。
(2)CO和H2S反应可产生羰基硫( COS)。在一恒容密闭容器中发生反应:CO(g)+H2S(g)![]() COS(g)+H2(g)并达到平衡,数据如下表所示:
COS(g)+H2(g)并达到平衡,数据如下表所示:
实验 | 温度/℃ | 起始时 | 平衡时 | |||
n(CO)/mol | n(H2S)/mol | n(COS)/mol | n(H2)/mol | n(CO)/mol | ||
1 | 150 | 10.0 | 10.0 | 0 | 0 | 7.0 |
2 | 150 | 7.0 | 8.0 | 2.0 | 4.5 | a |
3 | 400 | 20.0 | 20.0 | 0 | 0 | 16.0 |
①该反应是________反应(填“吸热”或“放热”)。
②实验1达平衡时,CO的转化率为_______。
③实验2达到平衡时,a_______7.0(填“大于”“小于”或“等于”)。
④实验3达平衡后,再充入1.0 molH2,平衡常数值____(填“增大”“减小”或“不变”)。
(3)COS是大气污染物。在酸性溶液中可用H2O2氧化COS生成一种强酸脱硫。该脱除反应的化学方程式为_______________。
(4)有一种脱硫工艺为:真空K2CO3一克劳斯法。
①K2CO3溶液吸收H2S的反应为K2CO3 +H2S =KHS +KHCO3,该反应的平衡常数的对数值为lgK=_____(已知:H2CO3 lgK1=-6.4,lgK,2=- 10.3;H2S lgKl=-7.0,lgK2
②已知下列热化学方程式:
a. 2H2S(g)+3O2(g)=2SO2(g)+2H2O(1) △H1=-1172kJ/mol
b. 2H2S(g)+O2(g)=2S(s)+2H2O(1) △H2 = 632 kJ/mol
克劳斯法回收硫的反应为SO2和H2S气体反应生成S(s),则该反应的热化学方程式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知一定条件下合成氨反应:N2(g)+3H2(g) ![]() 2NH3(g) ΔH=-92.4 kJ·mol-1 , 在反应过程中,反应速率的变化如图所示,请根据速率的变化回答采取的措施。
2NH3(g) ΔH=-92.4 kJ·mol-1 , 在反应过程中,反应速率的变化如图所示,请根据速率的变化回答采取的措施。
t1; t2; t3; t4。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2;元素Y基态原子的3p轨道上有4个电子.X与Y形成的化合物的晶胞如图所示,下列关于该晶体的说法正确的是( )
A.1个晶胞中离子的总数为18
B.X2+离子的配位数为8,Y2﹣离子的配位数为4
C.与每个X2+距离最近的X2+共有12个
D.该化合物的化学式为CaS
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某些药品可以明显增加运动员的兴奋程度。下列药品中属于国际奥委会严格禁止使用的兴奋剂的是( )。
A.碳酸镁 B.青霉素 C.阿司匹林 D.麻黄碱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,某体积不变的密闭容器中发生如下可逆反应:A2(g)+B2(g)![]() 2AB(g)。该反应达到平衡状态的标志是
2AB(g)。该反应达到平衡状态的标志是
A. A2、B2、AB的反应速率的比值为1:1:2
B. 容器内的总压强不随时间变化而变化
C. 单位时间内生成2nmolAB的同时生成nmolB2
D. 容器内混合气体的平均相对分子质量保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂将制革工业污泥中的铬元素以难溶物CrOH(H2O)5SO4的形式回收,工艺流程如下,其中硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+。

回答下列问题:
(1)4.8 mol/L的硫酸溶液密度为1.27g/cm3,该溶液中硫酸的质量分数是_______。
(2)H2O2的作用是将滤液Ⅰ中的Cr3+转化为Cr2O72-,写出此反应的离子方程式:______。
(3)常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
阳离子 | Fe3+ | Mg2+ | Al3+ | Cr3+ |
开始沉淀时的pH | 2.7 | — | — | — |
沉淀完全时的pH | 3.7 | 11.1 | 5.4(>8溶解) | 9(>9溶解) |
①Cr (OH)3溶解于NaOH溶液时反应的离子方程式是___________。
②加入NaOH溶液使溶液呈碱性,Cr2O72-转化为CrO42-。滤液Ⅱ中阳离子主要有______;但溶液的pH不能超过8,其理由是______________________________。
(4)钠离子交换树脂的反应原理为Mn++nNaR→MRn+nNa+,利用钠离子交换树脂除去滤液Ⅱ中的金属阳离子是_____________。
(5)写出上述流程中用SO2进行还原时发生反应的化学方程式:_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com