
��֪�� 2SO2��g��+O2��g��2SO3��g�� ��H=-196.0kJ��mol-1
2NO��g��+O2��g��2NO2��g�� ��H=-113.0kJ��mol-1
2SO3��l��2SO3��g�� ��H= 20.0 kJ��mol-1
��NO2��SO2��Ӧ����SO3��l����һ����ɫ������Ȼ�ѧ����ʽ ��
����һ�������£���NO2��SO2�������1:2���ں����ܱ������з���������Ӧ��
��������˵����Ӧ�ﵽƽ��״̬���� ��
a����ϵѹǿ���ֲ���
b�����������ɫ���ֲ���
c��SO3��NO������ȱ��ֲ���
d��ÿ����1mol SO3��ͬʱ����1 molNO2
�ڸ÷�Ӧ��ƽ��ʱ�����NO2��ת����Ϊ50%����Ӧǰ��������ѹǿ��Ϊ ��
�ۺ�ѹ�ܱ������з���������Ӧʱ��������Ar����ʹ�÷�Ӧ���� �����С�䣩��
SO2��g��+NO2��g��SO3��l��+NO��g�� ��H����51.5 kJ��mol-1
��a,b �� 6:5 �۱�С
����:�����˹���ɵ�Ӧ�á��ɷ�Ӧ��2SO2��g��+O2��g��2SO3��g�� ��H=-196.0kJ��mol-1����Ӧ��2NO��g��+O2��g��
2NO2��g����H=-113.0 kJ��mol-1�͢�2SO3��l��
2SO3��g�� ��H= 20.0 kJ��mol-1��֪�����٣��ڣ��۵�2SO2��g��+2NO2��g��
2SO3��l��+2NO��g�����������H����103kJ��mol-1��
����Ϊ��Ӧǰ������DZ仯�ģ����Ե�ѹǿ���ٱ仯ʱ������˵���Ѿ��ﵽƽ�⡣��ɫ����dz����Ũ�ȴ�С�йأ����Ե���ɫ���ٱ仯ʱ��Ҳ����˵���Ѿ��ﵽƽ��״̬������������Һ�壬C����ȷ����������1 mol SO3��ͬʱ��Ȼ����1 molNO2m������˵����
�� SO2��g��+NO2��g��SO3��l��+NO��g��
��ʼ����mol�� 2 1 0 0
ת������mol�� 0.5 0.5 0.5 0.5
ƽ������mol�� 1.5 0.5 0.5 0.5
��Ӧǰ��������ѹǿ��Ϊ![]() .
.
�ۺ�ѹ�ܱ������з���������Ӧʱ��������Ar�����������������Ȼ�������ʵ�Ũ�Ȼ��С����Ӧ�����͡�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
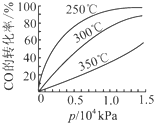 �о�NO2��SO2��CO�ȴ�����Ⱦ����Ĵ���������Ҫ���壮
�о�NO2��SO2��CO�ȴ�����Ⱦ����Ĵ���������Ҫ���壮| ���� |
| ���� |
| 8 |
| 3 |
| 8 |
| 3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
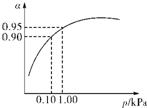 ����������Ҫ����Ƿ��������ȣ��������Ʒ����������������裮
����������Ҫ����Ƿ��������ȣ��������Ʒ����������������裮| ���� | �� | �� | �� |
| ��Ӧ��Ͷ���� | 2molSO2��1molO2 | 2molSO3 | mmolSO2��nmolO2��pmolSO3 |
| c��SO3��/mol?L-1 | 1.4 | 1.4 | 1.4 |
| �����仯 | �ų�akJ | ����bkJ | ����ckJ |
| SO2��SO3��ת���� | ��1 | ��2 | 12.5% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 2SO3��g������H=-197kJ/mol��ʵ����ij������4molSO2����������Ӧʱ�ų�275.8kJ��������SO2��ת���ʣ������ĵ�SO2ռԭ��SO2�İٷֱȣ�Ϊ
2SO3��g������H=-197kJ/mol��ʵ����ij������4molSO2����������Ӧʱ�ų�275.8kJ��������SO2��ת���ʣ������ĵ�SO2ռԭ��SO2�İٷֱȣ�Ϊ�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
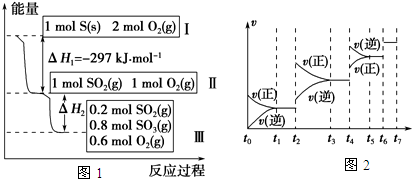
| t1-t2 | t3-t4 | t5-t6 | t6-t7 |
| K1 | K2 | K3 | K4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���� | SO2��mol�� | O2��mol�� | ������mol�� | ��ƽ��ʱʵ����ЧӦ��kJ?mol-1�� |
| �� | 2 | 1 | 0 | ��Hl |
| �� | 1 | 0.5 | 0 | ��H2 |
| �� | 1 | 0.5 | 1 | ��H3 |
| A����Hl=-197 kJ?mol-1 |
| B����H2=��H3 |
| C����Hl=2��H2 |
| D����Hl����H3 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com