
【题目】对于4NH3(g)+3O2(g)=2N2(g)+6H2O(g)的反应来说,以下化学反应速率的表示中反应速率最快的是( )
A.v(NH3)=0.6mol·L-1·s-1B.v(O2)=0.4mol·L-1·s-1
C.v(N2)=0.2mol·L-1·s-1D.v(H2O)=1.2mol·L-1·min-1
【答案】A
【解析】
对于反应4NH3(g)+3O2(g)=2N2(g)+6H2O(g),用不同物质表示其反应速率,数值不同但意义相同,所以比较反应速率要转化为同种物质的反应速率来比较大小,且反应速率之比等于化学计量数之比,以此来解答。
A.v(NH3)=0.6mol·L-1·s-1;
B.v(O2)=0.4mol·L-1·s-1,则v(NH3)=0.4mol·L-1·s-1×![]() =0.53 mol·L-1·s-1;
=0.53 mol·L-1·s-1;
C.v(N2)=0.2mol·L-1·s-1,则v(NH3)=0.2 mol·L-1·s-1×2=0.4mol·L-1·s-1;
D.v(H2O)=1.2mol·L-1·min-1,则v(NH3)=1.2mol·L-1·min-1×![]() =
=![]() mol·L-1·s-1;
mol·L-1·s-1;
显然A表示的该反应的反应速率最大,故选A。


 百年学典课时学练测系列答案
百年学典课时学练测系列答案科目:高中化学 来源: 题型:
【题目】十九大报告提出要对环境问题进行全面、系统的可持续治理。绿色能源是实施可持续发展的重要途径,利用生物乙醇来制取绿色能源氢气的部分反应过程如下图所示:
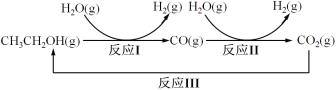
(1)已知:CO(g)+H2O(g)![]() CO2(g)+H2(g) △H1= - 41 kJ/mol
CO2(g)+H2(g) △H1= - 41 kJ/mol
CH3CH2OH(g)+3H2O(g)![]() 2CO2(g)+6H2(g) △H2=+174.1 kJ/mol
2CO2(g)+6H2(g) △H2=+174.1 kJ/mol
请写出反应I的热化学方程式_____________________________。
(2)反应II,在进气比[n(CO) : n(H2O)]不同时,测得相应的CO平衡转化率见下图
(各点对应的反应温度可能相同,也可能不同;各点对应的其他反应条件都相同)。

① 经分析,A、E和G三点对应的反应温度相同,其原因是KA=KE=KG=________(填数值)。在该温度下:要提高CO平衡转化率,除了改变进气比之外,还可采取的措施是________。
② 对比分析B、E、F三点,可得出对应的进气比和反应温度的变化趋势之间的关系是_____________________________________________________________。
③ 比较A、B两点对应的反应速率大小:VA______VB(填“<” “=”或“>”)。反应速率v=v正-v逆=![]() -
-![]() ,k正、k逆分别为正、逆向反应速率常数,x为物质的量分数,计算在达到平衡状态为D点的反应过程中,当CO转化率刚好达到20%时
,k正、k逆分别为正、逆向反应速率常数,x为物质的量分数,计算在达到平衡状态为D点的反应过程中,当CO转化率刚好达到20%时![]() =__________ (计算结果保留1位小数)。
=__________ (计算结果保留1位小数)。
(3)反应III,利用碳酸钾溶液吸收CO2得到饱和的KHCO3电解液,电解活化的CO2来制备乙醇。
①已知碳酸的电离常数Ka1=10-a,Ka2=10-b,吸收足量CO2所得饱和KHCO3溶液的pH=c,则该溶液中lg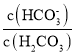 =____________________________________(列出计算式)。
=____________________________________(列出计算式)。
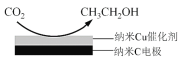
②在饱和KHCO3电解液中电解CO2来制备乙醇的原理如图所示。则阴极的电极反应式是_____________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物X的蒸气相对氢气的密度为51,X中氧元素的质量分数为31.7%,则能在碱性溶液中发生反应的X的同分异构体有(不考虑立体异构)( )
A. 12种B. 13种C. 14种D. 15种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用钛矿的酸性废液(含TiO2+、Fe2+、Fe3+、SO42-等),可回收获得FeS2纳米材料、Fe2O3和TiO2·nH2O等产品,流程如下:
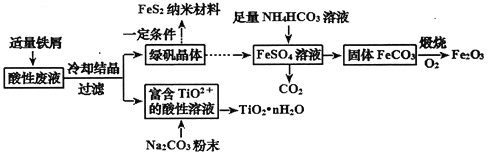
(1)TiO2+中钛元素的化合价为________价。TiO2+只能存在于强酸性溶液中,因为TiO2+易水解生成TiO2·nH2O,写出水解的离子方程式_________________________________。
(2)向富含TiO2+的酸性溶液中加入Na2CO3粉末能得到固体TiO2·nH2O。请用化学反应原理解释__________________________________。
(3)NH4HCO3溶液与FeSO4溶液反应的离子方程式为_______________________,该反应需控制温度在308K以下,其目的是_____________________________。
(4)已知298K时,Ksp[Fe(OH)2]=8.0×10-16,若在生成的FeCO3达到沉淀溶解平衡时,测得溶液的pH为8.5,c(Fe2+)=1.0×10-5mol·L-1,则所得的FeCO3中________Fe(OH)2(填“有”或“没有”)。
(5)FeS2纳米材料可用于制造高容量锂电池,已知电解质为熔融的K2S,电池放电时的总反应为:4Li+FeS2=Fe+2Li2S,则正极的电极反应式是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知甲、乙、丙三种物质均含有同种元素X,其转化关系如下:
![]()
下列说法错误的是
A.若A为NaOH溶液,乙为白色沉淀,则X可能为短周期金属元素
B.若A为硝酸,X为金属元素,则甲与乙反应可生成丙
C.若A为氧气,丙在通常状况下为红棕色气体,则甲可能为非金属单质
D.若乙为NaHCO3,则甲或丙可能是CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列各组物质或微粒:
①O2和O3;②12C和14C;③CH4和C7H16;④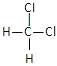 和
和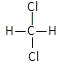 ;⑤
;⑤![]() 和
和![]() 。
。
(1)下列说法正确的是______。
A.①组两微粒互为同位素
B.②组互为同素异形体
C.③组两物质互为同系物
D.④组两物质互为同分异构体
E.⑤组互为同分异构体
(2)有机物![]() 的名称为______。
的名称为______。
(3)用一个Cl取代![]() 分中的一个氢原子可以得到______种结构不同的有机物。
分中的一个氢原子可以得到______种结构不同的有机物。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子检验的方法正确的是
A. 某溶液![]() 有白色沉淀,说明原溶液中有Cl-
有白色沉淀,说明原溶液中有Cl-
B. 某溶液![]() 有白色沉淀,说明原溶液中有SO42-
有白色沉淀,说明原溶液中有SO42-
C. 某溶液![]() 有蓝色沉淀,说明原溶液中有Cu2+
有蓝色沉淀,说明原溶液中有Cu2+
D. 某溶液![]() 生成无色气体,说明原溶液中有CO32-
生成无色气体,说明原溶液中有CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图表示细胞内某些有机物的元素组成和功能关系,其中A、B代表元素,Ⅰ、Ⅱ、Ⅲ、Ⅳ、Ⅴ是生物大分子,图中X、Y、Z、P分别为构成生物大分子的基本单位,请据图回答下列问题:
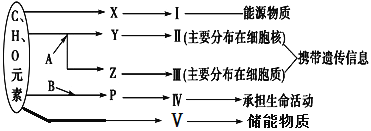
(1)图中A代表的元素是(用元素符号填写)_______________。图中X是_______________,Ⅰ在小麦种子中主要是指_______________。
(2)Ⅴ在动物、植物细胞均含有,是生物体内理想的储能物质,则Ⅴ是_______________。
(3)物质P是_______________,其结构通式为______________________________;若Ⅳ分子由n个P分子(平均相对分子质量为m)组成的2条链组成,则该Ⅳ分子的相对分子质量大约为______________。从理论上分析,该Ⅳ物质至少有_____个氨基和_____个羧基。
(4)生物体中的Ⅱ、Ⅲ的基本组成单位是__________各单位间是通过______________键连接起来的,可以通过___________________________对细胞进行染色,染色后Ⅱ呈现出_______色,Ⅲ呈现出_______色。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有NH3、CO、Na、Na2O2、Fe、NO、NO2、F2、SO2、SOCl2等物质,根据它们的组成及性质进行如下分类:
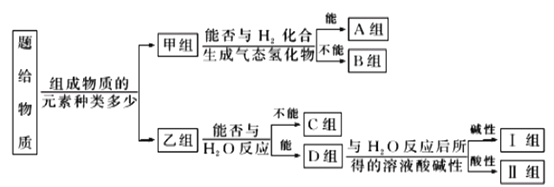
请回答下列问题:
(1)图中所示的分类方法叫___________。
(2)淡黄色固体最终位于__________组,它的电子式为___________。
(3)B组中有一种物质在高温下能与水蒸气反应,若该反应过程中有8×6.02×1023个电子转移,则有__g该物质参与反应。
(4)C组有一种气体常用作工业上冶炼铁的还原剂,写出高温下它还原Fe2O3的化学方程式___________。
(5)II组某种物质能与水发生氧化还原反应,该反应中被氧化元素与被还原的元素的质量比为___________。
(6)II组另有一种物质滴入水中后与水剧烈反应,元素化合价不发生变化,该物质与水反应的化学方程式___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com