
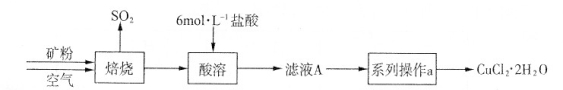
(共15分) 某矿样含有大量的CuS及少量其它不溶于酸的杂质。实验室中以该矿样为原料制备CuCl2·2H2O晶体,流程如下:
(1)在实验室中,欲用37%(密度为1.19 g·mL-1)的盐酸配制500 mL 6 mol·L-1的盐酸,需要的仪器除量筒、烧杯、玻璃棒外,还有_______________ 、 _______________ 。
(2)①若在实验室中完成系列操作a。则下列实验操作中,不需要的是_______ (填下列各项中序号)。

②CuCl2溶液中存在如下平衡:Cu(H2O)42+(蓝色)+4Cl- 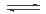 CuCl42-(黄色)+4H2O。
CuCl42-(黄色)+4H2O。
欲用实验证明滤液A(绿色)中存在上述平衡,除滤液A外,下列试剂中,还需要的是____ (填下列各项中序号)。 a.FeCl3固体 b.CuCl2固体 c.蒸馏水
(3)某化学小组欲在实验室中研究CuS焙烧的反应过程,查阅资料得知在空气条件下焙烧CuS时,固体质量变化曲线及SO2生成曲线如下图所示。

①CuS矿样在焙烧过程中,有Cu2S、CuO·CuSO4、CuSO4、CuO生成,转化顺序为下列四阶段:

第①步转化主要在200~300oC范围内进行,该步转化的化学方程式为 _______________ 。
②300~400oC范围内,固体质量明显增加的原因是_______________,上图所示过程中,CuSO4固体能稳定存在的阶段是__________(填下列各项中序号)。
a.一阶段 b、二阶段 c、三阶段 d、四阶段
③该化学小组设计如下装置模拟CuS矿样在氧气中焙烧第四阶段的过程,并验证所得气体为SO2和O2的混合物。

a.装置组装完成后,应立即进行气密性检查,请写出检查A-D装置气密性的操作 __________ 。
b.当D装置中产生白色沉淀时,便能说明第四阶段所得气体为SO2和O2的混合物。你认为装置D中原来盛有的溶液为_______________ 溶液。
c.若原CuS矿样的质量为l0.0 g(含加热不反应的杂质),在实验过程中,保持温度在760oC左右持续加热,待矿样充分反应后,石英玻璃管内所得固体的质量为8.4 g,则原矿样中CuS的质量分数为__________。
(共15分) (1)胶头滴管 500ml容量瓶(各1分)
(2)cd (1分) c(2分)
(3) 2CuS+O2 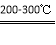 Cu2S+SO2 (2分)
Cu2S+SO2 (2分)
Cu2S转化为CuSO4 固体质量增加(2分) c(1分)
关闭分液漏斗活塞,在D中加水至淹没下端管口,微热A中圆底烧瓶看到D中有气泡冒出,停止微热后导管中有一小段水柱回流,则气密性好(2分)
BaCl2或其他合理答案(1分)
96.0﹪(2分)
【解析】
试题分析:(1)用液体配制溶液,需要量筒、烧杯、玻璃棒、胶头滴管、及容量瓶,本题中需配制500mL的溶液所以需要500mL的容量瓶;
(2)①从滤液到晶体,需要蒸发浓缩、冷却结晶、过滤步骤得到晶体,不需要灼烧、分液,所以答案选cd;
②欲用实验证明滤液A(绿色)中存在上述平衡,则需要改变条件,看是否有平衡移动,因此实验中加入水后溶液蓝色加深,即可证明存在平衡;不能加入氯化铁固体或氯化铜固体,原因是铁离子和铁离子本身有颜色,实验c正确;
(3)①200~300oC范围内进行的是第一阶段,所以产物主要是Cu2S,所以化学方程式为
2CuS+O2  Cu2S+SO2 ;
Cu2S+SO2 ;
②300~400oC范围内,进行的是第二阶段,主要产物是CuO·CuSO4,相当于固体中增加了氧元素的质量,所以固体质量明显增加;从图中可以看出,CuSO4固体能稳定存在的阶段是第三阶段,答案选c;
③A-D装置气密性的检查,利用温度升高,气体压强增大的原理检验,具体操作是:关闭分液漏斗活塞,在D中加水至淹没下端管口,微热A中圆底烧瓶看到D中有气泡冒出,停止微热后导管中有一小段水柱回流,则气密性好;证明第四阶段所得气体为SO2和O2的混合物,气体溶于溶液后可得硫酸根离子,所以只需验证硫酸根离子的存在即可,因此应选择氯化钡溶液;石英玻璃管内所得固体为CuO,其质量为8.4 g,物质的量是0.1mol,根据元素守恒,可得CuS的质量是9.6g,所以原矿样中CuS的质量分数为96%。
考点:考查物质制备,仪器的选择,装置气密性的检查,图像分析,质量分数的计算


科目:高中化学 来源:2013-2014甘肃省下学期期中考试高一化学试卷(解析版) 题型:选择题
银锌纽扣电池的总反应式为Zn+Ag2O+H2O = Zn(OH)2+2Ag,下列说法不正确的是( )
A.锌做负极 B.放电时,正极产物是银
C.电解质溶液不可能呈酸性 D.充电时发生了原电池反应
查看答案和解析>>
科目:高中化学 来源:2013-2014甘肃兰州一中高一下学期期末考试化学试卷(解析版) 题型:填空题
(10分)五种短周期元素A、B、C、D、E,原子序数逐渐增大,A、B处于同一周期,C、D、E同处另一周期。C、B可按原子个数比2∶l和1∶1分别形成两种离子化合物甲和乙。A原子的最外层电子数比次外层电子层多3个。E周期序数等于E原子最外层电子数。根据以上信息回答下列问题:
(1)A、B、C、D、E五种元素的原子半径由小到大的顺序是 (用元素符号填写)
(2)乙物质中存在的化学键类型是 。
(3)选用恰当的试剂除去D中少量的E,写出发生反应的化学方程式
(4)化合物乙的电子式
(5)将D、E的单质插入NaOH溶液中,构成原电池,其负极反应是
查看答案和解析>>
科目:高中化学 来源:2013-2014甘肃兰州一中高一下学期期末考试化学试卷(解析版) 题型:选择题
下列物质中,不能使酸性KMnO4溶液褪色的物质是
①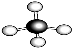 ②乙烯 ③CH3COOH;④CH3CH2OH ⑤CH2=CH—COOH ⑥
②乙烯 ③CH3COOH;④CH3CH2OH ⑤CH2=CH—COOH ⑥
A.①⑥B.①③④⑥C.①④D.①③⑥
查看答案和解析>>
科目:高中化学 来源:2013-2014甘肃兰州一中高一下学期期末考试化学试卷(解析版) 题型:选择题
许多国家十分重视海水资源的综合利用。不需要化学变化就能够从海水中获得的物质是
A.氯、溴、碘B.钠、镁、铝C.食盐、淡水D.烧碱、氢气
查看答案和解析>>
科目:高中化学 来源:2013-2014湖南长沙县一中、浏阳一中、宁乡一中高三5月化学试卷(解析版) 题型:选择题
要组装一套实验室利用液体和液体反应制备气体的装置,现设计了如下的五步操作,正确的程序是
①将蒸馏烧瓶固定在铁架台上
②将酒精灯放在铁架台上,根据酒精灯确定铁圈高度,固定铁圈,放好石棉网
③用漏斗向蒸馏烧瓶中加入一种液体反应物,再向分液漏斗中加入另一种液体反应物,并将导气管放入气体收集装置中
④检查装置的气密性(利用固定装置微热的方法检查气密性)
⑤在蒸馏烧瓶中装好分液漏斗,连接好导气管
A.②①⑤④③ B.④②①⑤③
C.②①⑤③④ D.①⑤④②③
查看答案和解析>>
科目:高中化学 来源:2013-2014湖南省长沙市高三高考二模理综化学试卷(解析版) 题型:填空题
【化学——选修2:化学与技术】(15分)
电镀厂镀铜废水中含有CN-和Cr2O72- 离子,需要处理达标后才能排放。该厂拟定下列流程进行废水处理,回答下列问题:

(1)上述处理废水流程中主要使用的方法是_________________;
(2)②中反应后无气体放出,该反应的离子方程式为______________;
(3)步骤③中,每处理0.4mol Cr2O72-时转移电子2.4mol,该反应的离子方程式为 ;
(4)取少量待测水样于试管中,加入NaOH溶液,观察到有蓝色沉淀生成,再加Na2S溶液,蓝色沉淀转化成黑色沉淀,请使用化学用语和文字解释产生该现象的原因 ;
(5)目前处理酸性Cr2O72-废水多采用铁氧磁体法。该法是向废水中加入FeSO4 ·7H2O将Cr2O72-还原成Cr3+,调节pH,Fe、Cr转化成相当于: (铁氧磁体,罗马数字表示元素价态)的沉淀。
(铁氧磁体,罗马数字表示元素价态)的沉淀。
处理1mol Cr2O72-,需加入a mol FeSO4 ? 7H2O,下列结论正确的是_______。
A. x =0.5 ,a =8 B. x =0.5 ,a = 10 C. x = 1.5 ,a =8D. x = 1.5 ,a = 10
查看答案和解析>>
科目:高中化学 来源:2013-2014湖南省衡南县高二下学期期末考试化学试卷(解析版) 题型:选择题
在2009年10月1日,新的饮用矿泉水强制性国家标准《饮用天然矿泉水》正式实施,其中“溴酸盐(BrO3-)”这一潜在致癌物质被做了严格限制。有关专家解释,矿泉水在开采过程中会含有少量溴化物(Br-),在后续的生产过程中经臭氧(O3)处理逐渐转化成溴酸盐。下列有关该转化过程的认识正确的是( )
A.该过程中溴化物(Br-)得到电子
B.该过程中臭氧(O3)是氧化剂,溴酸盐(BrO3-)是还原剂
C.该过程中溴元素被还原,氧元素被氧化
D.该过程中溴元素发生氧化反应,氧元素发生还原反应
查看答案和解析>>
科目:高中化学 来源:2013-2014湖南省衡南县高一下学期期末考试化学试卷(解析版) 题型:选择题
环境污染已成为人类社会面临的重大威胁,各种污染数不胜数。下列名词与环境污染无关的是
①温室效应 ②赤潮 ③酸雨 ④光化学污染 ⑤臭氧层空洞 ⑥水俣病 ⑦潮汐 ⑧大脖子病
A.①②③ B.⑦⑧ C.①⑤⑥ D.②⑤⑦
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com