
分析 (1)该有机物含有的官能团的名称是碳碳双键、羟基和羧基;
(2)酸能使紫色石蕊试液变红色,该羧基能和碳酸钠、碳酸氢钠反应生成气体;
(3)该物质中含有碳碳双键、羟基、羧基,具有烯烃、醇和羧酸性质;
(4)1mol该有机物完全与溴水发生加成反应时,有几摩尔碳碳双键,最多需要Br2几摩尔;
(5)醇羟基的检验要根据醇羟基的性质来进行,避开双键和羧基的干扰.
解答 解:(1)该有机物含有的官能团的名称是碳碳双键、羟基和羧基,故答案为:碳碳双键、羟基和羧基;
(2)含有-COOH的羧酸具有酸的通性:可以使紫色石蕊试液变红,和碳酸钠、碳酸氢钠反应生成二氧化碳,故答案为:紫色石蕊试液;变红(或NaHCO3、Na2CO3溶液,有气体生成);
(3)A.羧基和羟基都能与金属Na反应放出氢气,故正确;
B.碳碳双键与Cl2能发生加成反应,连接羧基的亚甲基能发生取代反应,故错误;
C.只有羧基能和NaOH反应,则1mol该有机物可与1mol NaOH反应,故错误;
D.碳碳双键在一定条件能与H2发生加成反应,故正确;
故选AD;
(4)1mol该有机物完全与溴水发生加成反应时,有几摩尔碳碳双键,最多需要Br2几摩尔,该物质中含有2个碳碳双键,所以1mol该有机物完全与溴水发生加成反应时,需要Br2 2mol,故答案为:2;
(5)醇羟基的检验要根据醇羟基的性质:和金属反应放氢气、能使酸性高锰酸钾溶液褪色,但是碳碳双键也能使酸性高锰酸钾溶液褪色,所以要避开双键的干扰,
故答案为:取少量该有机物加入适量溴水,使碳碳双键完全反应,再加入少量酸性高锰酸钾溶液,溶液褪色则说明含醇羟基.
点评 本题考查有机物结构和性质,为高频考点,明确官能团及其性质关系是解本题关键,侧重考查烯烃、醇和羧酸性质,易错点是醇羟基的检验,要排除其它官能团的干扰,题目难度不大.


 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案科目:高中化学 来源: 题型:选择题
| A | B | |
| 实验 方案 | 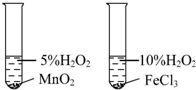 | 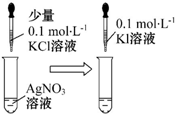 |
| 实验 目的 | 比较不同催化剂对同一反应速率的影响 | 证明:Ksp(AgCl)>Ksp(AgI) |
| C | D | |
| 实验 方案 | 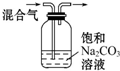 | 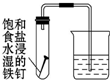 |
| 实验 目的 | 除去CO2气体中混有的SO2 | 证明铁钉生锈过程中有氧气参与反应 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 环己醇分子中所有的原子可能共平面 | |
| B. | 按系统命名法,(CH3CH2)2CHCH3化合物的名称是3-乙基丁烷 | |
| C. | 芳香化合物A(C8H8O3)分子中含有酯基和醚键两种含氧官能团,A可能的同分异构体有4种 | |
| D. | 在一定条件下,1.0 mol的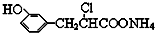 最多能与含4.0 mol NaOH的溶液完全反应 最多能与含4.0 mol NaOH的溶液完全反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
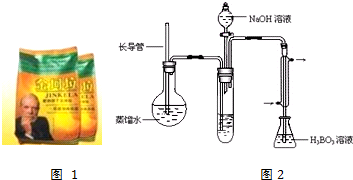
| 实验编号 | 样品和辅助试剂 | 消耗盐酸体积(mL) |
| 1 | 10.00mL溶液、0.2g催化剂、20mL浓硫酸 | 33.45 |
| 2 | 10.00mL溶液、0.2g催化剂、20mL浓硫酸 | 33.90 |
| 3 | 10.00mL溶液、0.2g催化剂、20mL浓硫酸 | 33.50 |
| 4 | x |
| 级别 | 优等品 | 一等品 | 合格品 |
| 总尿素含量%≥ | 46.4 | 46.2 | 46.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
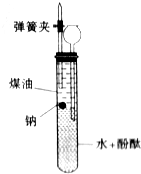
 现有一瓶标签受到腐蚀(如图所示)的无色溶液,已知该溶液可能是碳酸钠、碳酸氢钠、氯化钠、硫酸钠、硝酸钠、硫化钠中的一种,为确定溶液的成分,同学们进行了如下探究:
现有一瓶标签受到腐蚀(如图所示)的无色溶液,已知该溶液可能是碳酸钠、碳酸氢钠、氯化钠、硫酸钠、硝酸钠、硫化钠中的一种,为确定溶液的成分,同学们进行了如下探究:查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 向FeI2溶液中通入少量氯气:2Fe2++Cl2═2Fe3++2Cl- | |
| B. | 将少量CO2通入NH3•H2O中:CO2+2NH3•H2O═(NH4)2CO3+H2O | |
| C. | 将少量SO2通入NH3•H2O中:SO2+2NH3•H2O═(NH4)2SO3+H2O | |
| D. | 将AlCl3与等量Na2CO3溶液混合:3H2O+Al3++CO32-═HCO3-+Al(OH)3+2H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (1)等质量的O2、CH4、H2的物质的量的比值为1:2+16.
(1)等质量的O2、CH4、H2的物质的量的比值为1:2+16.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验内容 | 试剂 | 实验现象 |
| 验证氧化性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com