
| A.1 mol H2O的质量为18g/mol | B.标准状况下,1 mol任何物质体积均为22.4L |
| C.CH4的摩尔质量为16g | D.3.01×1023个SO2分子的质量为32g |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
| A.22.4 L氨气中含氢原子数目为3×6.02×1023 |
| B.1.8g水中所含质子数为0.1×6.02×1023 |
| C.标准状况下,4.48 L的氧气和氮气的混合物含有的分子数目为0.2×6.02×1023 |
| D.80 g苛性钠溶于1L水中,所得溶液的物质的量浓度为2 mol/L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.4︰7 | B.10︰7 | C.14︰11 | D.11︰14 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.10m1 、0.1mol·L-1的AlC13溶液 | B.20m1、 0.1mo1·L-1的CaC12溶液 |
| C.30m1、 0.2mo1·L-1的KC1溶液 | D.100m1 、0.25mo1·L-1的NaC1溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.取用6.4 g CuSO4溶解于200 mL 水中 |
| B.若取出100 mL该溶液,Cu2+的浓度为0.1 mol ∕ L |
| C.配制该浓度的CuSO4溶液,需CuSO4·5H2O 10 g |
| D.最终所配成的溶液中含有Cu2+个数为3.01×1022 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
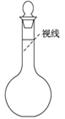
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.500 mol/L | B.1. 00 mol/L | C.2. 00 mol/L | D.3. 00 mol/L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com