
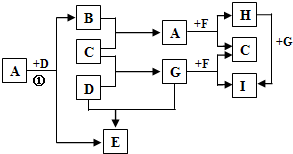
有A、B、C、D.E、F六种含六个以内碳原子的含氧衍生物,它们的质量组成均含C 40%,含H 6.67%;燃烧等物质的量的A、B、C、D生成的CO2体积比为6∶2∶1∶3,燃烧等物质的量的E、F生成水的物质的量比为1∶3,A、B、C、F均可发生银镜反应,D、E显酸性,D在铜作催化剂时在空气中加热可反应,但产物不发生银镜反应,推断出A、B、C、D、E、F各是什么物质?
科目:高中化学 来源: 题型:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com