
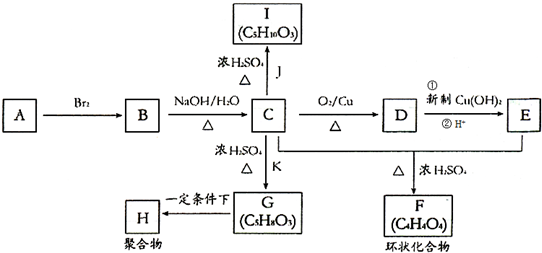
 ,由G的分子式可知,乙二醇与丙烯酸发生酯化反应生成G,K为CH2=CHCOOH,G为CH2=CHCOOCH2CH2OH,由I的分子式可知,乙二醇与CH3CH2COOH发生酯化反应生成I,J为CH3CH2OH,I为CH3CH2COOCH2CH2OH,据此解答.
,由G的分子式可知,乙二醇与丙烯酸发生酯化反应生成G,K为CH2=CHCOOH,G为CH2=CHCOOCH2CH2OH,由I的分子式可知,乙二醇与CH3CH2COOH发生酯化反应生成I,J为CH3CH2OH,I为CH3CH2COOCH2CH2OH,据此解答. ,由G的分子式可知,乙二醇与丙烯酸发生酯化反应生成G,K为CH2=CHCOOH,G为CH2=CHCOOCH2CH2OH,由I的分子式可知,乙二醇与CH3CH2COOH发生酯化反应生成I,J为CH3CH2OH,I为CH3CH2COOCH2CH2OH,
,由G的分子式可知,乙二醇与丙烯酸发生酯化反应生成G,K为CH2=CHCOOH,G为CH2=CHCOOCH2CH2OH,由I的分子式可知,乙二醇与CH3CH2COOH发生酯化反应生成I,J为CH3CH2OH,I为CH3CH2COOCH2CH2OH, ;F的结构简式为
;F的结构简式为 ,故答案为:
,故答案为: ;
; ;
;| Cu |
| △ |
| 一定条件 |
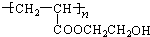 ,
,| Cu |
| △ |
| 一定条件 |
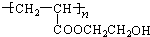 ;
;

 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③④ | B、①③⑤ |
| C、②④⑥ | D、②⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
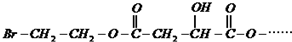 已知:X在足量的氢氧化钠水溶液中加热,可得到A、B、C三种有机物.
已知:X在足量的氢氧化钠水溶液中加热,可得到A、B、C三种有机物.
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、9~11之间;0.1 |
| B、9~11之间;0.05 |
| C、12~13之间;0.2 |
| D、13;0.1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
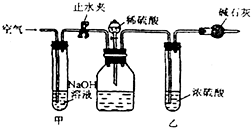
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、盐酸 |
| B、FeCl3 |
| C、Fe(NO3)3 |
| D、BaCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、化学反应速度:乙>甲 |
| B、平衡后O2的浓度:乙>甲 |
| C、SO2的转化率:乙>甲 |
| D、平衡后SO2的百分含量:乙>甲 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com