
硫酸锶(SrSO4)在水中的沉淀溶解平衡曲线如图,下列说法正确的是
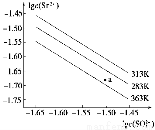
A.283 K时,图中a点对应的溶液是不饱和溶液
B.三个不同温度下,363 K时Ksp(SrSO4)最大
C.温度一定时,Ksp(Sr SO4)随c(SO)的增大而减小
SO4)随c(SO)的增大而减小
D.283 K下的SrSO4饱和溶液升温到363 K后变
为不饱和溶液
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2016届浙江省嘉兴、杭州、宁波五校高三上第一次联考化学试卷(解析版) 题型:选择题
在某温度时,将nmol/L的氨水滴入10mL0.1mol/L盐酸中,溶液pH和温度随加入氨水体积变化曲线如图所示。下列有关说法正确的是
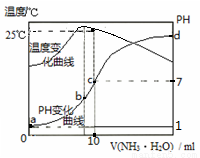
A.a点KW=1.0×10-14
B.水的电离程度:b>c>a>d
C.b点:c(NH4+)>c(Cl-)>c(H+)>c(OH-)
D.25℃时,一水合氨的电离平衡常数为10-7/(10n-1)(用n表示)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东广州执信中学高二上期中文化学试卷(解析版) 题型:?????
鉴别织物成分是真蚕丝还是“人造丝”,在如下①-④的各方法中正确的是(  )
)
①滴加浓硝酸 ②滴加浓硫酸 ③滴加酒精 ④灼烧
A.①和③ B.③和④ C.①和④ D.①和②
查看答案和解析>>
科目:高中化学 来源:2016届内蒙古巴彦淖尔市高三上期中考试理化学试卷(解析版) 题型:实验题
某研究性学习小组为测定某含镁3%一5%的铝镁合金(不含其它元素)中镁的质量分数,设计了下列三种不同实验方案进行探究,请根据他们的设计回答有关问题。
【探究一】实验方案:将铝镁合金 测定剩余固体质量。
测定剩余固体质量。
问题讨论:
(1)实验中发生反应的化学方程式是 。
(2)若实验中称取5.4g铝镁合金粉末样品,投入VmL2.0mol/L NaOH溶液中,充分反应。则NaOH溶液的体积V≥ mL。
(3)实验中,当铝镁合金充分反应后,在称量剩余固体质量前,还需进行的实验操作按顺序依次为 。
【探究二】实验方案:称量xg铝镁合金粉末,放在如图所示装置的惰性电热板上,通电使其充分灼烧。
问题讨论:
(4)欲计算Mg的质量分数,该实验中还需测定的数据是 。
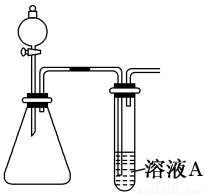
(5)假设实验中测出该数据为yg,则原铝镁合金粉末中镁的质量分数为 (用含x、y代数式表示)。
[探究三]实验方案:镁铝合金 测定生成气体的体积。
测定生成气体的体积。
问题讨论:
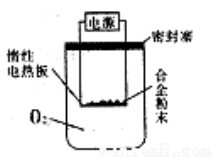
(6)同学们拟选用下边的实验装置完成实验,你认为最简易的装置其连接顺序是:a接 。(填接口字母,仪器不一定全选。)
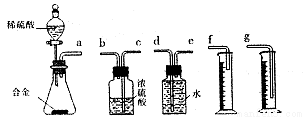
(7)同学们仔细分析(6)中连接的实验装置后,又设计了下左图所示的实验装置。
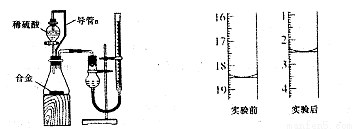
①装置中导管a的作用是 。
②实验前后碱式滴定管中液面读数分别如上右图,则产生氢气的体积为 mL。
③与上左图装置相比,用(6)中连接的装置进行实验时,容易引起误差的原因是 (任写一点)。
查看答案和解析>>
科目:高中化学 来源:2016届贵州省高三第五次模拟理科综合试卷(解析版) 题型:填空题
要配制450mL 0.2mol•L-1FeSO4溶液,实验操作步骤有:①在天平上称取a g绿矾(FeSO4•7H2O),将它放在烧杯中,用适量蒸馏水使其完全溶解 ②将所得溶液沿玻璃棒注入500mL容量瓶中 ③继续向容量瓶中加水至液面距刻度线1–2cm处,改用胶头滴管滴加蒸馏水至凹液面底部与刻度线相切 ④用少量水洗涤烧杯和玻璃棒2-3次,每次洗液都转入容量瓶 ⑤将容量瓶塞紧,充分摇匀
填写下列空白
(1)a g绿矾的实际质量为____________g。
(2)上述操作步骤的正确顺序为__________________。
(3)下列操作会使所配溶液的浓度偏高的是__________。
A.若配制时遗漏步骤④; B.定容时俯视刻度线;
C.称量时物、码放反了; D.绿矾样品已部分风化
E.摇匀后溶液低于刻度线,再加入蒸馏水使液面最低点与刻度线相切;
F.引流时玻璃棒靠在刻度线上方
(4)取一定体积所配制硫酸亚铁的溶液,用一定浓度的酸性KMnO4标准溶液进行滴定,滴定过程中______(需要或不需要)指示剂,并说明理由_________________________________________。
Ⅱ. 三氟化氮(NF3)是一种新型的电子材料,它在潮湿的空气中与水蒸气能发生氧化还原反应,其生成物有HF、NO、HNO3。根据要求回答下列问题:
(1)写出该反应的化学方程式:_________________________________________。反应过程中,被氧化与被还原的元素物质的量之比为______。
(2)若反应中生成0.2mol HNO3,转移的电子数目为______。
查看答案和解析>>
科目:高中化学 来源:2016届福建省三明市高三上学期第二次月考化学试卷(解析版) 题型:选择题
下列说法不正确的是
A.医用酒精的浓度通常为75%
B.用灼烧并闻气味的方法区别纯棉织物和纯毛织物
C.采集某雨水样品,放置一段时间,pH由4.8变为4.2,是因为水中溶解了较多的CO2
D. 氢氧化铝和碳酸氢钠都可以作为治疗胃酸过多的药剂
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南二校高一理科实验班上联考2化学卷(解析版) 题型:选择题
将一定量的镁和铜组成的混合物加入到稀硝酸中,金属完全溶解(假设反应中还原产物只有NO)。向反应后的溶液中加人3 mol/L NaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1 g。则下列叙述中不正确的是( )
A.当生成的沉淀量达到最大时,消耗NaOH溶液的体积V≥100 mL
B.当金属全部溶解时,参加反应的硝酸的物质的量一定是0.4mol
C.参加反应的金属的总质量为9.6 g>m>3.6 g
D.当金属全部溶解时收集到NO气体的体积一定为2.24 L。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建三明一中高一上学期第二次月考化学卷(解析版) 题型:选择题
关于Na2CO3和NaHCO3性质的说法不正确的是
A.在水中的溶解性:NaHCO3<Na2CO3
B.相同条件下,与等浓度盐酸反应生成CO2的速率:NaHCO3<Na2CO3
C.等质量的Na2CO3和NaHCO3分别与足量盐酸反应,NaHCO3放出CO2更多
D.等物质的量的Na2CO3和NaHCO3分别与足量 盐酸反应产生的CO2质量相同
盐酸反应产生的CO2质量相同
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二上期中测试化学试卷(解析版) 题型:选择题
在一定温度下,10mL0.40mol/LH2O2发生催化分解。不同时刻测定生成O2的体积(已折算为标准状况)如下表。
t/min | 0 | 2 | 4 | 6 | 8 | 10 |
V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
下列叙述不正确的是(溶液体积变化忽略不计)
A.0~6 min的平均反应速率:v(H2O2)≈3.3×10-2 mol/(L•min)
B.6~10 min的平均反应速率:v(H2O2)<3.3×10-2 mol/(L•min)
C.反应到6 min时,c(H2O2)=0.30mol/L
D.反应到6 min时,H2O2分解了50%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com