
| A. | 一定含有I-,不能确定是否含有Cl- | B. | 一定含有NO3- | ||
| C. | 不含有Fe3+,可能含有NO3- | D. | 一定含有I-、NO3-和Cl- |
 全能测控一本好卷系列答案
全能测控一本好卷系列答案 发散思维新课堂系列答案
发散思维新课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 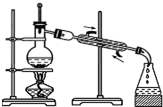 分离沸点相差较大液体混合物 | B. | 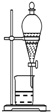 分离互不相溶的两种液体 | ||
| C. | 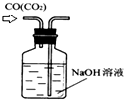 除去CO气体中的CO2气体 | D. | 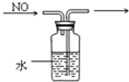 排水集气法收集NO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Si→SiO2→H2SiO3→Na2SiO3 | |
| B. | Al→Al2O3→Al(OH)3→NaAlO2 | |
| C. | Na→Na2O→Na2O2→NaOH→Na2CO3→NaHCO3 | |
| D. | S→SO3→H2SO4→SO2→Na2SO3→Na2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 盐酸浓度不变,使用量增大1倍 | B. | 盐酸浓度增加1倍,但用量减至1/2 | ||
| C. | 将碳酸钙固体改为碳酸钙粉末 | D. | 加热此反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol Cl2溶于水的过程中有1NA个电子转移 | |
| B. | 标准状况下,22.4L NO2气体中含有NA个O2分子 | |
| C. | 常温常压下,15g HCHO含有2NA对共用电子对 | |
| D. | 1L 0.1mol•L-1的醋酸溶液中有NA个CH3COO- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
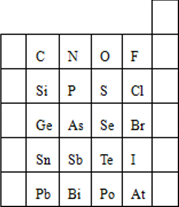 元素在周期表中的位置,反映了元素的原子结构和元素的性质.如图是元素周期表的一部分.
元素在周期表中的位置,反映了元素的原子结构和元素的性质.如图是元素周期表的一部分.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ④③①⑤ | B. | ③⑥⑤① | C. | ②③① | D. | ②③⑤① |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com