
| A. | 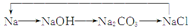 | B. | 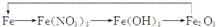 | ||
| C. |  | D. | 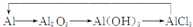 |
分析 Na、Mg、Al、Fe能和酸反应生成盐,能被氧化性强的单质氧气氧化生成氧化物,再结合复分解反应条件来分析解答,注意氧化物和碱之间的转化.
解答 解:A.Na→NaOH→Na2CO3→NaCl中反应方程式分别为:2Na+2H2O=2NaOH+H2↑、2NaOH+CO2=Na2CO3 +H2O、Na2CO3+CaCl2=CaCO3↓+2NaCl,电解熔融的氯化钠得到单质钠,所以能全部是通过一步反应完成,故A不选;
B.Fe→Fe(NO3)3→Fe(OH)3→Fe2O3中反应分别是Fe$\stackrel{过量的硝酸}{→}$Fe(NO3)3$\stackrel{氢氧化钠}{→}$Fe(OH)3$\stackrel{加热}{→}$Fe2O3$\stackrel{还原剂}{→}$Fe,所以全部是通过一步反应完成,故B不选;
C.Mg→Mg(OH)2→MgSO4中反应方程式分别为:镁与水微弱反应生成氢氧化镁、Mg(OH)2+H2SO4=MgSO4+2H2O,硫酸镁与氯化钡反应生成氯化镁,电解熔融的氯化镁得到单质镁,全部是通过一步反应完成,故C不选;
D.氧化铝和水不反应,所以不能一步生成氢氧化铝,故D选;
故选D.
点评 本题考查了物质间的转化,明确物质的性质是解本题关键,根据物质的性质来分析解答,以Na、Mg、Al、Fe为知识点构建知识网络,元素化合物知识常常在工艺流程中出现,还常常与基本实验操作、物质的分离与提纯、离子的检验等知识点联合考查,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | Al3+、Ba2+、Cl-、NO3- | B. | K+、OH-、Cl-、SO42- | ||
| C. | Ca2+、Mg2+、NO3-、HCO3- | D. | Na+、Cl-、CO32-、SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某温度时在2L容器中X、Y、Z三种气态物质的物质的量(n)随时间(t)变化的曲线如图所示,由图中数据分析:
某温度时在2L容器中X、Y、Z三种气态物质的物质的量(n)随时间(t)变化的曲线如图所示,由图中数据分析:查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 物质 | Al | Al2O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2054 | 1535 | 1462 |
| 沸点/℃ | 2467 | 2980 | 2750 | -- |
 (4)图中OC段没有沉淀生成,此阶段发生反应的离子方程式为H++OH-═H2O.
(4)图中OC段没有沉淀生成,此阶段发生反应的离子方程式为H++OH-═H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通入足量CO2后的溶液中:Na+、SiO32-、CH3COO-、CO32- | |
| B. | 中性溶液中:Fe3+、MnO4-、SO42-、K+ | |
| C. | 酸性溶液中:Na+、ClO-、SO42-、I- | |
| D. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=1012的溶液中:NH4+、Al3+、NO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| A组 | B组 | C组 | D组 |
| 金刚石:3550 | Li:181 | HF:-83 | NaCl:801 |
| 硅晶体:1410 | Na:98 | HCl:-115 | KCl:776 |
| 硼晶体:2300 | K:64 | HBr:-89 | RbCl:718 |
| 二氧化硅:1723 | Rb:39 | HI:-51 | CaCl:645 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用水鉴别乙醇、甲苯和溴苯 | |
| B. | 用燃烧法鉴别乙醇、苯 | |
| C. | 用碳酸钠溶液鉴别乙醇、乙酸和乙酸乙酯 | |
| D. | 用酸性高锰酸钾溶液鉴别苯、环己烯和环己烷 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com