

���� ��1����A���Ȼ�������������ڼ��������·�Ӧ���ɰ������Ȼ��ƺ�ˮ��
�ڰ���Ϊ�������壬c�лӷ��İ�������ˮ����������E����ǰӦ���и��Ӧѡ����Ը������
��2���ٵ�NOx��Na2CO3��Һ��ȫ����ʱ����n��NO2����n��NO�����Դ˼���x��
����ͼ��֪��xx=1.5����Һ�����ɵ�NO3-��NO2-�������ӣ�aΪ���bΪ��С���������ﻯѧʽ��֪��NaNO3��NaNO2�е�Ԫ������Ԫ��֮��Ϊ1��1��
�����ò���������NO��NO2�����ʵ������ٸ���ƽ��Ħ������������xֵ��
��3�����������ж����Ի�������Ⱦ��
��4�������������V��NO����V��NO2��=5��1ʱ��Ӧͨ��һ�����������ﵽ���������V��NO����V��NO2��=1��1��
��� �⣺��1���ٵ��������������ɹ⻯ѧ�������ʴ�Ϊ����ɹ⻯ѧ���� ���������꣩��
��A���Ȼ�������������ڼ��������·�Ӧ���ɰ������Ȼ��ƺ�ˮ������ʽ��2NH4Cl+Ca��OH��2 $\frac{\underline{\;\;��\;\;}}{\;}$CaCl2+2NH3��+2H2O��
�ʴ�Ϊ��2NH4Cl+Ca��OH��2 $\frac{\underline{\;\;��\;\;}}{\;}$CaCl2+2NH3��+2H2O��
�ۼ�ʯ��Ϊ���Ը����������Ϊ�������壬���Կ����ü�ʯ�Ҹ��ﰱ����
�ʴ�Ϊ����ȥ�����к��е�ˮ������
��2�����ɷ���ʽ��֪��NO�������ܱ����գ�NO��NO2������屻NaOH��Һ����ȫ���գ�����n��NO2����n��NO����1����n��NO2����n��NO��=1ʱxֵ��С��x��СֵΪ$\frac{1+2}{2}$=1.5����Ϊ����NO������x���ֵ��2����x��ȡֵ��ΧΪ1.5��x��2������x��ֵ��������1.3��
�ʴ�Ϊ��A��
���ü�������x=1.5����ӦΪNO��NO2�������ʵ�����Ϊ1��1����NO+NO2+Na2CO3�T2NaNO2+CO2��Ӧ��û��NO3-����aӦ�ñ�ʾNO2-��
���غ㷨��֪����Ӧ���ɵ�NaNO3��NaNO2�е�Ԫ������Ԫ��֮��Ϊ1��1������1mol NOx����ȫ����������̼����0.5mol������Ϊ53g������̼������Һ������Ϊ$\frac{53g}{21.2%}$=250g��
�ʴ�Ϊ��NO2-��250��
������NO2�ʹ��Ӧ����CO2Ϊamol��
��NO��NO2�봿�Ӧ������CO2Ϊbmol��
2NO2+Na2CO3=NaNO2+NaNO3+CO2���������ӡ�m=48g
1mol 48g
amol 48ag
NO+NO2+Na2CO3=2NaNO2+CO2���������ӡ�m=32g
1mol 32g
bmol 32bg
$\left\{\begin{array}{l}{a+b=1}\\{48a+32b=44}\end{array}\right.$��
���a=0.75mol��b=0.25mol��
n��NO2��=0.75mol��2+0.25mol=1.75mol
n��NO��=0.25mol
x=$\frac{0.25mol��1+1.75mol��2}{0.25mol+1.75mol}$=1.875��
�ʴ�Ϊ��1.875��
��3�����������ж����Ի�������Ⱦ���ô������յ��������ܽ��ж�����ת��Ϊ�����ʣ���ֹ�ж��������Ⱦ��
�ʴ�Ϊ�����ж�����ת��Ϊ�����ʣ���ֹ�ж��������Ⱦ��
��4�������������V��NO����V��NO2��=5��1ʱ������NOΪ5mol��NO2Ϊ1mol��Ϊʹ���屻��ȫ���գ�Ӧ����NOΪ3mol��NO2Ϊ3mol�����跴Ӧ2molNO����NO2��
�ɷ���ʽ2NO+O2=2NO2��֪����Ҫ1molO2���ֿ������������������ԼΪ20%������Ҫ5mol������
����V����������V��NO��=5��5=1��1��
�ʴ�Ϊ��1��1��
���� �����Ե�������Ϊ���忼�������ʼ�ķ�Ӧ����ȷ���ʵ������ǽⱾ��ؼ����ѵ��ǣ�2������ļ��㣬Ҫ��Ϸ���ʽ�и���������֮��Ĺ�ϵʽ��𣬻���������Ϣ����xֵ���Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
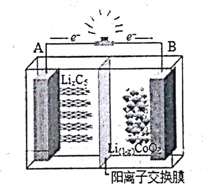 ����ͼΪҡ�ڵ�أ�Rocking chair battery���Ĺ���ԭ��ͼ���ڳ�ŵ�����У�Li+������֮�䡰ҡ��ҡȥ�������ܷ�ӦΪ��LiCoO2+6C$?_{�ŵ�}^{���}$Li��1-x��CoO2+LixC6�������й�˵����ȷ���ǣ�������
����ͼΪҡ�ڵ�أ�Rocking chair battery���Ĺ���ԭ��ͼ���ڳ�ŵ�����У�Li+������֮�䡰ҡ��ҡȥ�������ܷ�ӦΪ��LiCoO2+6C$?_{�ŵ�}^{���}$Li��1-x��CoO2+LixC6�������й�˵����ȷ���ǣ�������| A�� | �ŵ�ʱ��������ӦLiCoO2-xe-�TLi��1-x��CoO2+Li+ | |
| B�� | ���ʱ��A������������Ӧ | |
| C�� | ���ʱ��Li+��������Ĥ��B���ƶ� | |
| D�� | ��B��ʧȥxmol���ӣ������1molLiCoO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ع��;����ӹ��������������Ʒ������������ | |
| B�� | PM2.5��������ֱ��ԼΪ2.5��10-6m����ɢ�ڿ������γ����ܽ� | |
| C�� | ��������TiO2�ⴥý�������ɽ�װ�������ͷŵ�HCHOת��Ϊ������ | |
| D�� | ����ʮһ�ŷɴ�����̫���ܵ�ذ�ɽ�����ת��Ϊ���ܣ�����ת�������ǹ辧�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| �������� | Fe��OH��3 | Fe��OH��2 | Ni��OH��2 |
| ��ʼ������pH | 1.1 | 6.5 | 7.1 |
| ������ȫ��pH | 3.2 | 9.7 | 9.2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 28gN2����ԭ����ΪNA | B�� | 0.5molH2O����ԭ����Ϊ1.5NA | ||
| C�� | 1molH2O���е�ˮ������ĿΪNA | D�� | 0.5NACl2���ӵ����ʵ�����0.5mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 3-������
3-������ 2��2-����-3-�һ����飮
2��2-����-3-�һ����飮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ | B�� | ŨH2SO4 | C�� | ��ˮCaCl2 | D�� | ��ʯ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
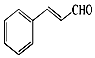 ��Ȼ���е�����ֲ���к���ȩ��������Щ�����������ζ������Ϊֲ������ʹ�ã���Ƥ�к������ȩ���ṹ��ͼ�������к��б���ȩ������˵��������ǣ�������
��Ȼ���е�����ֲ���к���ȩ��������Щ�����������ζ������Ϊֲ������ʹ�ã���Ƥ�к������ȩ���ṹ��ͼ�������к��б���ȩ������˵��������ǣ�������| A�� | ���ȩ�����к������ֹ����ţ�����ʽΪC9H8O | |
| B�� | ���ȩ�����������18��ԭ�ӹ�ƽ�� | |
| C�� | 1 mol���ȩ�������ӳ�ʱ�������4 mol H2 | |
| D�� | ���ȩ�뱽��ȩ����ͬϵ������ܷ���������Ӧ�ͻ�ԭ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
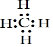 �� B��D��ɵ���ԭ�ӷ��ӵĽṹʽΪO=C=O��
�� B��D��ɵ���ԭ�ӷ��ӵĽṹʽΪO=C=O���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com