

分析 硼镁矿与氢氧化钠溶液反应,过滤除去杂质,NaBO2溶液中,通入过量的二氧化碳,得到Na2B4O7•10H2O与为NaHCO3,过滤分离,由于硼酸的酸性小于硫酸,符合复分解反应由强酸制弱酸的原理,且硼酸的溶解度较小,故Na2B4O7•10H2O晶体与硫酸反应得到硼酸,溶液b中含有硫酸钠,硼酸晶体加热分解得到B2O3,最后用Mg还原得到粗硼.
(1)根据化合价代数和为0计算B元素化合价;
(2)由上述分析可知,第①步通入过量二氧化碳,则a为NaHCO3,第③步加入硫酸,b为Na2SO4;
(3)第①步为Mg2B2O5.H2O与氢氧化钠溶液反应生成NaBO2与Mg(OH)2;
(4)步骤⑤是Mg与B2O3发生置换反应生成B与MgO;
(5)符合复分解反应由强酸制弱酸的原理;
(6)乙硼烷在空气中燃烧生成B2O3与水.
解答 解:硼镁矿与氢氧化钠溶液反应,过滤除去杂质,NaBO2溶液中,通入过量的二氧化碳,得到Na2B4O7•10H2O与为NaHCO3,过滤分离,由于硼酸的酸性小于硫酸,符合复分解反应由强酸制弱酸的原理,且硼酸的溶解度较小,故Na2B4O7•10H2O晶体与硫酸反应得到硼酸,溶液b中含有硫酸钠,硼酸晶体加热分解得到B2O3,最后用Mg还原得到粗硼.
(1)根据化合价代数和为0,可知Mg2B2O5•H2O中B的化合价为+3,
故答案为:+3;
(2)由上述分析可知,第①步通入过量二氧化碳,则a为NaHCO3,第③步加入硫酸,b为Na2SO4,
故答案为:NaHCO3;Na2SO4;
(3)第①步为Mg2B2O5.H2O与氢氧化钠溶液反应生成NaBO2与Mg(OH)2,反应方程式为:Mg2B2O5•H2O+2NaOH=2NaBO2+2Mg(OH)2,
故答案为:Mg2B2O5•H2O+2NaOH=2NaBO2+2Mg(OH)2;
(4)步骤⑤是Mg与B2O3发生置换反应生成B与MgO,反应方程式为:B2O3+3Mg$\frac{\underline{\;\;△\;\;}}{\;}$2B+3MgO,
故答案为:B2O3+3Mg$\frac{\underline{\;\;△\;\;}}{\;}$2B+3MgO;
(5)步骤③中化学反应可以发生的原因是:硼酸的酸性小于硫酸,符合复分解反应由强酸制弱酸的原理,且硼酸的溶解度较小,从溶液中析出有利于该反应的进行,
故答案为:硼酸的酸性小于硫酸,符合复分解反应由强酸制弱酸的原理,且硼酸的溶解度较小,从溶液中析出有利于该反应的进行;
(6)乙硼烷在空气中燃烧生成B2O3与水,反应方程式为:B2H6+3O2$\frac{\underline{\;点燃\;}}{\;}$B2O3+3H2O,
故答案为:B2H6+3O2$\frac{\underline{\;点燃\;}}{\;}$B2O3+3H2O.
点评 本题考查化学制备方案,理解工艺流程原理是解题关键,侧重对化学用语的考查,需要学生具备扎实的基础与灵活运用的能力,难度中等.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向AlCl3溶液中滴加氨水,产生白色沉淀;再加入过量NaHSO4溶液,沉淀消失 | |
| B. | 向盛有Fe(NO3)2溶液的试管中加入0.1 mol•L-1H2SO4溶液,试管口出现红棕色气体,说明溶液中NO3-被Fe2+还原为NO2 | |
| C. | 将某气体通入品红溶液中,品红褪色,说明该气体一定是SO2 | |
| D. | 将CO2通入BaCl2溶液中至饱和,无沉淀产生;再通入SO2,产生沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有①②③ | B. | 只有①⑤ | C. | 只有③④⑤ | D. | 只有②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将80 g NaOH溶于2 L 水所得的溶液 | |
| B. | 将0.5 mol•L-1的NaNO3溶液100 mL 加热蒸发掉50 g水所得的溶液 | |
| C. | 将40 g NaOH 溶于水并配成1 L的溶液 | |
| D. | 含K+为4 mol•L-1的K2SO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 一定状态的分子 | H2(g) | Br2(l) | HBr(g) |
| 1mol该分子中的化学键断裂吸收的能量/kJ | 436 | a | 369 |
| A. | 404 | B. | 344 | C. | 260 | D. | 200 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液中四种粒子之间不可能满足:c(C1-)>c(H+)>c(NH4+)>c(OH-) | |
| B. | 若溶液中粒子间满足:c(NH4+)>c(C1-)>c(OH-)>c(H+)则溶液中溶质一定为:NH4Cl和NH3•H2O,且溶液pH>7 | |
| C. | 若溶液中粒子间满足:c(C1-)>c(NH4+)>c(H+)>c(OH-)溶液中溶质可能是NH4Cl | |
| D. | 若溶液中c(NH4+)=c(Cl-),则该溶液一定显中性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1L0.1mol•L-1FeCl3溶液中含有的Fe3+离子数目为0.1NA | |
| B. | 常温常压下,4.6gNO2和N2O4混合物中含有的原子总数为0.3NA | |
| C. | 1mol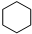 (环己烷)中含有6NA共价键 (环己烷)中含有6NA共价键 | |
| D. | 常温下,2.24LCl2完全与NaOH溶液反应,转移的电子数目一定为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
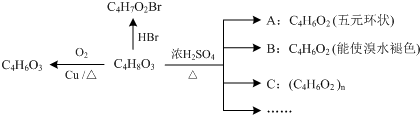
 .
. +H2O.
+H2O. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com