
科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:
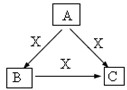 A、B、C、X是中学化学常见物质,均由短周期元素组成,转化关系如图.请针对以下三种不同情况回答:
A、B、C、X是中学化学常见物质,均由短周期元素组成,转化关系如图.请针对以下三种不同情况回答:查看答案和解析>>
科目:高中化学 来源:2004全国各省市高考模拟试题汇编·化学 题型:013
用相同质量的20% BaCl2溶液可使相同质量的FeSO4和CuSO4两种溶液中的硫酸根离子完全转化为沉淀,则这两种硫酸盐溶液的质量分数之比为
[ ]
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)下列实验操作或对实验事实的叙述正确的是______(填序号)。
①用稀HNO3清洗做过银镜反应实验的试管;
②配制浓硫酸和浓硝酸的混合酸时,将浓硫酸沿器壁慢慢加入到浓硝酸中,并不断搅拌;
③用碱式滴定管量取20.00 mL 0.1000 mol·L-1KMnO4溶液;
④用托盘天平称取10.50 g干燥的NaCl固体;
⑤不慎将苯酚溶液沾到皮肤上,立即用酒精清洗;
⑥用瓷坩埚高温熔融Fe(CrO2)2和Na2CO3的固体混合物;
⑦向沸腾的NaOH稀溶液中滴加FeCl3饱和溶液,以制备Fe(OH)3胶体;
⑧配制Al2(SO4)3溶液时,加入少量的稀硫酸。
(2)为了确定乙醇分子的结构简式是CH3—O—CH3?还是CH3CH2OH,实验室利用图2-3所示的实验装置,测定乙醇与钠反应(ΔH<0=生成氢气的体积,并据此计算乙醇分子中能与金属钠反应的氢原子的数目。试回答下列问题:

图2-3
①指出实验装置中的错误________________。
②若实验中用含有少量水的乙醇代替相同质量的无水乙醇,相同条件下,测得的氢气体积将_______(填“偏大”“偏小”或“不变”)。
③请指出能使该实验安全、顺利进行的关键实验步骤(至少指出两个关键步骤)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com