
回答下列问题
(1)在2FeBr2+3Cl2=2FeCl3+2Br2的反应中,被氧化的元素是_____________
(2)铁钉在氯气中被锈蚀成棕褐色物质FeCl3,而在盐酸中生成淡绿色溶液(FeCl2);浓盐酸中滴加KMnO4溶液产生黄绿色气体(Cl2)则Cl2、Fe3+、MnO4-氧化性由强到弱的顺序是____________________。
(3)已知CuO具有氧化性,能够和氨气反应生成物中有两种单质,请写出在加热条件下CuO和NH3反应的化学方程式___________________________
(4)实验室中的Na2SiO3溶液长期放置,瓶底会出现白色沉淀,形成沉淀的离子方程式是 。取瓶中的上层清液滴入稀盐酸,既有气泡又有沉淀生成,其离子方程式为 ,
(5)向大气中排放NOx可能导致的环境问题有____________________(答两点)
已知足量NaOH溶液能完全吸收NO2生成两种氮的含氧酸盐.试写出该反应的离子方程式
科目:高中化学 来源: 题型:
对于某些离子的检验及结论一定正确的是
A.加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32-
B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42-
C.加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+
D.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+
查看答案和解析>>
科目:高中化学 来源: 题型:
有如下图所示转化关系,A是一种常见的氧化物,D是非金属气体单质,其余是几种常见的有机物,其中G是“限塑令”禁用塑料袋的主要成分,F具有香味。
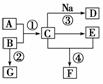

请回答下列问题:
(1)反应①、②的反应类型分别是________、________。
 (2)写出有机物E的结构简式_______
(2)写出有机物E的结构简式_______ _____。
_____。
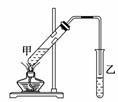
(3)实验室制取F的实验装置 如右图所示,该实验中加热试管的目的是:____________、________________________________。
如右图所示,该实验中加热试管的目的是:____________、________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关氯元素的单质及化合物的性质说法正确的是
A.液氯和氯水是纯净物,而漂白粉是混合物
B.氯气可用作消毒剂和漂白剂,是因为次氯酸具有强氧化性
C.实验室制取氯气时,可用饱和Na2CO3溶液除去其中的HCl
D.久置后的氯水酸性变弱
查看答案和解析>>
科目:高中化学 来源: 题型:
Na2FeO4是一种高效多功能水处理剂,应用前景十分看好。一种制备Na2FeO4的方法可用化学方程式表示如下:2FeSO4 + 6Na2O2 = 2Na2FeO4 + 2Na2O + 2Na2SO4 + O2↑,对此反应下列说法中正确的是
A.Na2O2只作氧化剂 B.FeSO4只作还原剂
C.铁元素被还原
D.2 mol FeSO4发生反应时,反应中共有8 mol电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质中一定互为同系物的是
A.CH2=CH2和CH2=CH-CH=CH2 B.C2H4和C6H12
C. (CH3)2CHCH(CH3)2和(CH3)2CHCH2CH(CH3)2 D. C2H6和C4H8
查看答案和解析>>
科目:高中化学 来源: 题型:
酒后驾车是引发交通事故的重要原因。公安部交通管理局新修订的《机动车驾驶证申领和使用规定》于2010年4月1日起正式实行,对酒后驾车加倍处罚,一次性扣12分。交警对驾驶员进行呼气酒精检测的原理是:橙色的K2Cr2O7酸性水溶液与乙醇反应,迅速生成蓝绿色的Cr3+。下列对乙醇的描述与此测定原理有关的是( )
①乙醇沸点低 ②乙醇密度比水小 ③乙醇有还原性 ④乙醇是烃的含氧化合物
A.②④ B.②③ C.①③ D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
A是一种重要的化工原料,A的产量通常用衡量一个国家石油化工发展水平标志。E是具有果香气味的烃的衍生物。A、B、C、D、E在一定条件下存在如下转化关系(部分反应条件、产物被省略)。
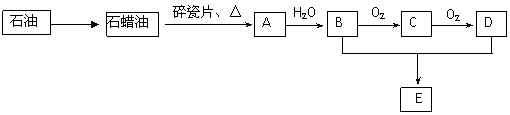
(1)工业上,由石油获得石蜡油的方法是 ;
(2)丁烷是由石蜡油获得A的过程中的中间产物之一,它的一种同分异构体中含有三个甲基,则这种同分异构体的结构简式是: ;
(3)A→B的化学方程式是: 该反应的反应类型是 ;
(4)B→C的化学方程式为: 该反应的反应类型是 ;
(5)反应B+D→E的反应的速率比较缓慢,我们在实验中为了提高该反应的速率,通常采取的措施有: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
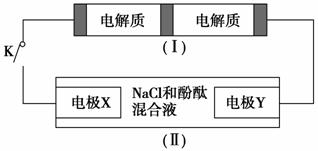
如图装置Ⅰ是一种可充电电池,装置Ⅱ为电解池。装置Ⅰ的离子交换膜只允许Na+通过,已知电池充放电的化学方程式为:2Na2S2+NaBr3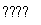 Na2S4+3NaBr,当闭合开关K时,X电极附近溶液变红。下列说法正确的是 ( )。
Na2S4+3NaBr,当闭合开关K时,X电极附近溶液变红。下列说法正确的是 ( )。
A.闭合开关K时,钠离子从右到左通过离子交换膜
B.闭合开关K时,负极反应式为:3NaBr-2e-===NaBr3+2Na+
C.闭合开关K时,X电极反应式为:2Cl--2e-===Cl2↑
D.闭合开关K时,当有0.1 mol Na+通过离子交换膜时,X电极上放出标准状
况下气体1.12 L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com