
工业上制备纯硅的热化学方程式如下:SiCl4(g)+2H2(g)  Si(s)+4HCl(g)ΔH=+Q kJ·mol-1 (Q>0);某温度、压强下,将一定量反应物通入密闭容器进行反应,下列叙述正确的是 ( )
Si(s)+4HCl(g)ΔH=+Q kJ·mol-1 (Q>0);某温度、压强下,将一定量反应物通入密闭容器进行反应,下列叙述正确的是 ( )
A.反应过程中,若增大压强能提高SiCl4的转化率
B.若反应开始时SiCl4为1 mol,则在平衡时,吸收热量为Q kJ
C.将反应的温度由T1升高至T2,则对应温度下的 平衡常数K1>K2
平衡常数K1>K2
D.当反应吸收热量为0.25Q kJ时,生成的HCl恰好与1 mol NaOH反应
科目:高中化学 来源:2016-2017学年广东佛山一中高二上第一次段考化学卷(解析版) 题型:实验题
下面是某同学测定化学反应速率并探究其影响因素的实验。
Ⅰ.测定化学反应速率
该同学利用如图装置测定化学反应速率。

(已知:S2O32-+2H+ = H2O+S↓+SO2↑)
(1)除如图所示的实验用品、仪器外,还需要的一件实验仪器是__________________。
(2)若在2 min时收集到224 mL(已折算成标准状况)气体,可计算出该2 min内H+的反应速率,而该测定值比实际值偏小,其原因是 。
(3)试简述测定该反应的化学反应速率的其他方法: (写一种)。
Ⅱ.为探讨化学反应速率的影响因素,设计的实验方案如下表。
(已知 I2+2S2O32- = S4O62-+2I-,其中Na2S2O3溶液均足量)
实验序号 | 体积V/mL | 时间/s | |||
Na2S2O3溶液 | 淀粉溶液 | 碘水 | 水 | ||
① | 10.0 | 2.0 | 4.0 | 0.0 | t1 |
② | 8.0 | 2.0 | 4.0 | 2.0 | t2 |
③ | 6.0 | 2.0 | 4.0 | Vx | t3 |
(4 )该实验进行的目的是 ,淀粉溶液的作用是 ,表中Vx= mL,通过比较t1、t2、t3大小,试推测该实验结论:
)该实验进行的目的是 ,淀粉溶液的作用是 ,表中Vx= mL,通过比较t1、t2、t3大小,试推测该实验结论: 
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东佛山一中高二上第一次段考化学卷(解析版) 题型:选择题
25℃、101kPa下,4g CH4完全燃烧生成CO2和液态H2O时,放出222.5 kJ的热量,则下列热化学方程式中正确的是 ( )
A.CH4(g)+2O2(g)=CO2(g)+4H2O(g) ΔH=-890 kJ/m ol
ol
B.CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=+890 kJ/mol
C.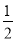 CH4(g)+O2(g)=
CH4(g)+O2(g)=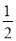 CO2(g)+H2O(l) ΔH=-445 kJ/mol
CO2(g)+H2O(l) ΔH=-445 kJ/mol
D.CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-890 kJ
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东佛山一中高二上第一次段考化学卷(解析版) 题型:选择题
对可逆反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g),下列叙述正确的是
4NO(g)+6H2O(g),下列叙述正确的是
A.2v正(NH3)=3v正(H2O)
B.达到化学平衡时,4v正(O2)=5v逆(NO)
C.达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大
D.若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com