
【题目】室温时,CaCO3在水中的溶解平街曲线如图所示。已知25℃ 其浓度积为2.8×10-9mol2/L2,下列说法不正确的是( )
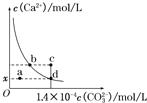
A.x数值为2×10-5 B.c点时有碳酸钙沉淀生成
C.加入蒸馏水可使溶液由d 点变到a点 D.b点与d对应的溶度积相等
科目:高中化学 来源: 题型:
【题目】已知A2On2-可将B2-氧化为B单质,A2On2-则被还原为A3+,又知100mL的0.3mol/L的A2On2-与150mL的0.6mol/L B2-恰好完全反应,则A2On2-中的n值为
A.4 B.5 C.6 D.7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室以一种工业废渣(主要成分为MgCO3、MgSO4和少量Fe、Al的氧化物)为原料制备MgCO33H2O。实验过程如下:
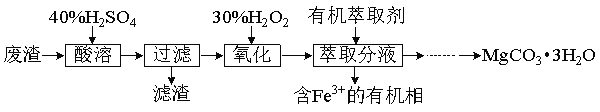
(1)酸溶需加热的目的是 ;过滤时用到的玻璃仪器有 ;
(2)加入H2O2氧化时发生发应的离子方程式为 。
(3)用如图所示的实验装置进行萃取和分液,以除去溶液中的Fe3+。
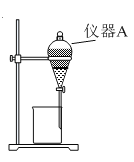
①实验装置图中仪器A的名称为 。
②为使Fe3+尽可能多地从水相转移至有机相,采取的操作:向装有溶液的仪器A中加入一定量的有机萃取剂, 、静置、分液,并重复多次。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将2.32 g Na2CO3、NaOH的固体混合物完全溶解于水,制成溶液,然后向该溶液中缓慢逐滴加入浓度为 0.1 mol/L的盐酸,所加盐酸的体积与产生CO2的体积(标准状况)关系如下图所示,下列说法中错误的是( )
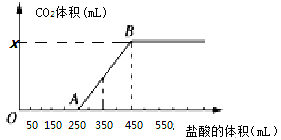
A.OA段发生反应的离子方程式为:H++OH-===H2O CO+H+===HCO
B.当加入350 mL盐酸时,产生CO2的体积为224 mL(标准状况)
C.x点对应的数值是448
D.混合物中NaOH的质量为1克
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活、环境有着密切的关系。
(1)光导纤维的主要成分是_________(填化学式)
(2)工业上制造水泥、玻璃和高炉炼铁都要用到的原料是________(填字母)
A.纯碱 B.石英 C.黏土 D.石灰石
(3)铝元素在人体中积累可使人慢性中毒,1989年世界卫生组织正式将铝确定为食品污染源之一而加以控制。铝及其化合物在下列场合使用时必须严格加以控制的是________(填字母)
A.用明矾净水 B.制电线电缆 C.制包糖果用的铝箔 D.制防锈油漆
(4)铝在空气中会被氧化生成一层致密的氧化膜(氧化物)而对铝起保护作用,但这层氧化膜(氧化物)遇到强酸或强碱都会溶解,请写出氧化膜与氢氧化钠溶液反应的化学方程式:_____________________
(5)工业上从海水中提取溴单质,可向海水中通入Cl2,将其中的溴化物氧化,离子方程式为____________________
(6)如图为实验室中盐酸试剂瓶标签上的部分内容。试回答下列问题:

①该盐酸的c(HCl)为_________ mol/L
②欲用该盐酸配制1.19 mol/L的盐酸480 mL。完成下列有关操作中的空白。
a.用_________(填实验仪器名称)准确量取盐酸,注入烧杯中,加入适量的水,混合均匀;
b.将操作a所得的盐酸沿玻璃棒注入_________mL容量瓶中;
c.用适量的水洗涤烧杯、玻璃棒2~3次,洗涤液均注入容量瓶中,振荡;
d.缓缓地将蒸馏水注入容量瓶中,直到瓶中的液面接近容量瓶的刻度线l~2cm处,改用_______________加蒸馏水至溶液的凹液面正好与刻度线相切;
e.将容量瓶盖好,反复上下颠倒摇匀。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cu(OH)2在水中存在着如下沉淀溶解平衡:Cu(OH)2(s) ![]() Cu2+(aq)+2OH-(aq),在常温下,Ksp=2×10-20。某CuSO4溶液中,c(Cu2+)=0.02 mol·L-1,在常温下如果要生成Cu(OH)2沉淀,需要向CuSO4溶液加入碱溶液来调整pH,使溶液的pH大于( )
Cu2+(aq)+2OH-(aq),在常温下,Ksp=2×10-20。某CuSO4溶液中,c(Cu2+)=0.02 mol·L-1,在常温下如果要生成Cu(OH)2沉淀,需要向CuSO4溶液加入碱溶液来调整pH,使溶液的pH大于( )
A.2 B.3 C.4 D.5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)请用下列10种物质的序号填空:①O2②H2③NH4NO3④K2O2⑤Ba(OH)2⑥CH4⑦CO2⑧NaF ⑨NH3⑩I2
既有离子键又有非极性键的是________;既有离子键又有极性键的是________。
(2)X、Y两种主族元素能形成XY2型化合物,已知XY2中共有38个电子,若XY2为常见元素形成的离子化合物,其电子式为:______________;若XY2为共价化合物时,其结构式为:__________________。
(3)氯化铝的物理性质非常特殊,如:氯化铝的熔点为190℃(2.02×103Pa),但在180℃就开始升华,据此判断,氯化铝是________(填“共价化合物”或“离子化合物”),可以证明你的判断正确的实验依据是____________________。
(4)现有a~g 7种短周期元素,它们在周期表中的位置如下,请据此回答下列问题:

①元素的原子间反应最容易形成离子键的是________(填序号,下同),容易形成共价键的是______;
A.c和f | B.b和g | C.d和g | D.b和e |
②写出a~g 7种元素形成的所有原子都满足最外层为8电子结构的任意一种分子的分子式______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com