
【题目】天然食用香料X是芳香族化合物,可以从某些植物中提取。由X合成H的路线如下:

已知:①A的核磁共振氢谱有6个峰;②H为酯类物质,结构中除苯环外还含有一个六元环;③G的产量是衡量一个国家石油化工发展水平的标志。
请回答下列问题:
(1)A的结构简式为______,检验A中非含氧官能团所用的试剂为_______。
(2)②的反应类型为____________。反应③的化学方程式为_____________。
(3)F中所含官能团的名称为____________,其同分异构体中,遇FeCl3溶液发生显色反应,且能与碳酸氢钠溶液反应,其苯环上一氯代物只有一种,符合条件的同分异构体数目为________种,写出其中一种结构简式:____________。
(4)设计一条以G为起始原料合成乙二酸的路线______________,无机物任选,注明反应条件。示例如下: ![]()
【答案】 ![]() 溴水(或溴的CCl4溶液) 加成反应
溴水(或溴的CCl4溶液) 加成反应 ![]() 羟基、羧基 2
羟基、羧基 2  或
或  H2CCH2
H2CCH2![]() BrH2CCH2Br
BrH2CCH2Br![]() HOCH2CH2OH
HOCH2CH2OH![]() OHCCHO
OHCCHO![]() HOOCCOOH
HOOCCOOH
【解析】G的产量是衡量一个国家石油化工发展水平的标志,则G为CH2=CH2,根据B的分子式可知B为CH3CH2OH,B发生消去反应生成乙烯。X在酸性条件下水解得到A与乙醇,则A为羧酸,A的核磁共振氢谱有6个峰,且能与HCl发生加成反应生成D,可知A为![]() ,故X为
,故X为![]() 。A与HCl发生加成反应生成D,D发生水解反应生成E,再酸化得到F,H为酯类结构,结构中除苯环外还含有一个六元环,说明F分子中羧基、羟基连接同一碳原子上,故D为
。A与HCl发生加成反应生成D,D发生水解反应生成E,再酸化得到F,H为酯类结构,结构中除苯环外还含有一个六元环,说明F分子中羧基、羟基连接同一碳原子上,故D为 ,E为
,E为 ,F为
,F为 ,H为
,H为 。则(1)A的结构简式为
。则(1)A的结构简式为![]() ,检验A中非含氧官能团碳碳双键时可利用其能与溴发生加成反应而使溴水或溴的四氯化碳溶液褪色,所用的试剂为溴水或溴的CCl4溶液;(2)反应②是A与HCl发生加成反应,反应③是乙醇在浓硫酸催化下发生消去反应生成乙烯,其化学方程式为
,检验A中非含氧官能团碳碳双键时可利用其能与溴发生加成反应而使溴水或溴的四氯化碳溶液褪色,所用的试剂为溴水或溴的CCl4溶液;(2)反应②是A与HCl发生加成反应,反应③是乙醇在浓硫酸催化下发生消去反应生成乙烯,其化学方程式为![]() ;(3)F中所含氧官能团为羟基、羧基,其同分异构体中,遇FeCl3溶液发生显色反应说明含有酚羟基,能与碳酸氢钠溶液反应说明含有羧基,其苯环上一氯代物只有一种可能取代基在对位,符合条件的同分异构体只有
;(3)F中所含氧官能团为羟基、羧基,其同分异构体中,遇FeCl3溶液发生显色反应说明含有酚羟基,能与碳酸氢钠溶液反应说明含有羧基,其苯环上一氯代物只有一种可能取代基在对位,符合条件的同分异构体只有 或
或 2种;(4)乙烯与溴发生加成反应生成1,2-二溴乙烷,1,2-二溴乙烷在强碱的水溶液中加热水解生成乙二醇,乙二醇催化氧化生成乙二醛,乙二醛进一步氧化可得乙二酸,则合成路线可设计如下:
2种;(4)乙烯与溴发生加成反应生成1,2-二溴乙烷,1,2-二溴乙烷在强碱的水溶液中加热水解生成乙二醇,乙二醇催化氧化生成乙二醛,乙二醛进一步氧化可得乙二酸,则合成路线可设计如下:
H2CCH2![]() BrH2CCH2Br
BrH2CCH2Br![]() HOCH2CH2OH
HOCH2CH2OH![]() OHCCHO
OHCCHO![]() HOOCCOOH
HOOCCOOH


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
【题目】在下图各物质的相互转化关系中:甲、乙、丙为三种金属单质;A、C、D常温下为气体,其中C呈黄绿色;G为白色沉淀;H为红褐色沉淀;B溶液焰色反应显黄色。(图中部分反应条件及生成物未全部标出)

填写下列空格:
(1)反应①的化学反应方程式___________________________________________
(2)F的化学式_________________
(3)写出B溶液与单质乙反应的化学方程式_________________________________
(4)C气体与F溶液反应的离子方程式_____________________________________
(5)写出实验室制备C气体的化学方程式____________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知温度T时水的离子积常数为KW。该温度下,将浓度为a mol/L的一元酸HA与b mol/L的一元碱BOH等体积混合,可判定该溶液呈中性的依据是
A.a = b
B.混合溶液的pH = 7
C.混合溶液中,c(H+) = ![]() mol/L
mol/L
D.混合溶液中,c(H+) +c(B) = c(OH) + c(A)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,夹子开始处于关闭状态,将液体A滴入试管②与气体B充分反应,打开夹子,可发现试管①内的水立刻沸腾了,则液体A和气体B的组合不可能是下列的

A. 氢氧化钠溶液、二氧化碳 B. 水、氨气 C. 氢氧化钠溶液、一氧化氮 D. 水、二氧化氮
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4CO(g)+2NO2(g)![]() N2(g)+4CO2(g)开始进行时,CO的浓度为4 mol/L,N2的浓度为0,2 min后测得N2的浓度为0.6 mol/L,则此段时间内,下列反应速率表示正确的是
N2(g)+4CO2(g)开始进行时,CO的浓度为4 mol/L,N2的浓度为0,2 min后测得N2的浓度为0.6 mol/L,则此段时间内,下列反应速率表示正确的是
A.v(CO)=1.2 mol/(L·s) B.v(NO2)=0.3 mol/(L·min)
C.v(N2)=0.6 mol/(L·min) D.v(CO2)=1.2 mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,二氧化硫和氧气发生如下反应:
2SO2(g)+O2(g)![]() 2SO3(g)+Q (Q>0)
2SO3(g)+Q (Q>0)
(1)写出该反应的化学平衡常数表达式K=_________.
(2)降低温度,该反应K值_________,二氧化硫转化率_________,正反应速度_________.(以上均填增大、减小或不变)
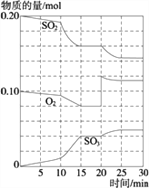
(3)600℃时,在一密闭容器中,将二氧化硫和氧气混合,反应过程中SO2、O2、SO3物质的量变化如图,反应处于平衡状态的时间是_________.
据图判断,反应进行至20 min时,曲线发生变化的原因_____________________(用文字表达);10 min到15 min的曲线变化的原因可能是_________(填写编号).
A.加了催化剂 B.缩小容器体积
C.降低温度 D.增加SO3的物质的量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20 mL0.1 mol L-1 Na2CO3溶液中逐滴加入0.1 mol L-1HCl溶液40 mL,溶液中含碳元素的各种微粒(CO2因逸出未画出)的物质的量浓度的百分含量随溶液pH变化的情况如下图所示。下列说法正确的是( )
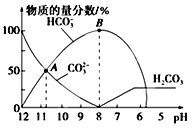
A. A点所处的溶液中c(Na+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-)
B. 随着盐酸的加入,溶液中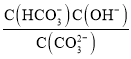 将减小
将减小
C. 随着盐酸的加入,当pH约为6时,溶液中开始放出气体
D. 当溶液的pH为7时,溶液的总体积为40mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.以Zn和Cu为电极,稀H2SO4为电解质溶液形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下:
①Zn为正极,Cu为负极
②H+向负极移动
③Cu极有H2产生
④电子流动方向Zn→Cu
⑤正极的电极反应式是Zn-2e-=Zn2+
⑥若有1mol电子流过导线,则理论上产生0.5 mol H2
(1)卡片中记录合理的是___________(填序号)
(2)该电池总反应的离子方程式是___________________________
(3)若将稀硫酸换成硫酸铜溶液,电极质量增加的是_____________ (填“锌极”或“铜极”)
Ⅱ.某温度时,在2 L密闭容器中,三种气态物质X、 Y、Z的物质的量(n)随时间(t)变化的曲线如右图所示,可得:
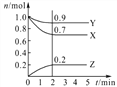
(1)该反应的化学方程式为_____________________
(2)反应开始至2 min,用Y表示的平均反应速率 为_______________
(3)在一定温度下,上述反应达到反应限度的标志的是____________
A. X、Y、Z的浓度相等
B. X、Y、Z的分子数比为3︰1︰2
C. Z的生成速率是Y的生成速率的二倍
D.单位时间内生成n mol Y,同时生成3n mol X
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com