
| A.同一元素各核素的质量数不同,但它们的化学性质几乎完全相同 |
| B.任何元素的原子都是由核外电子和核内中子、质子构成的 |
| C.钠原子失去一个电子后,它的电子数与氖原子相同,变成10e-微粒 |
D.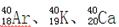 的质量数相同,所以它们互为同位素 的质量数相同,所以它们互为同位素 |
科目:高中化学 来源:不详 题型:单选题
| A | | C |
| | B | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
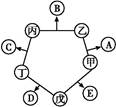
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
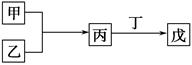
| A.若组成甲、乙的元素位于同一周期,则戊可能是一种弱酸 |
| B.若组成甲、乙的元素位于同一主族,则戊可能是一种弱酸 |
| C.若甲为短周期中原子半径最大的主族元素形成的单质,且戊为碱,则丙只能为Na2O2 |
| D.若丙、丁混合生成白烟,且丙为18电子分子,丁为10电子分子,则乙的水溶液可能具有漂白作用 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com