
【题目】实验室用浓硝酸氧化C2H2制取H2C2O4·2H2O的装置如图所示(电石主要成分为CaC2,含少量CaS杂质),下列说法正确的是( )
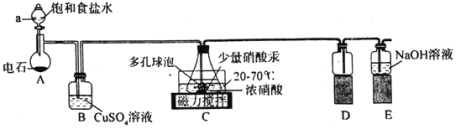
A.装置A可作MnO2和浓盐酸反应制备Cl2的发生装置
B.装置B的作用是除去C2H2中的H2S
C.装置D的作用是收集草酸
D.装置E中发生反应的离子方程式为3NO2+2OH-=2NO3-+NO+H2O
科目:高中化学 来源: 题型:
【题目】某同学模拟工业制碘的方法,探究ClO3-和I-的反应规律。实验操作及现象如下:
实验及试剂 | 编号 | 无色NaClO3溶液用量 | 试管中溶液颜色 | 淀粉KI试纸颜色 |
| 1 | 0.05mL | 浅黄色 | 无色 |
2 | 0.20mL | 深黄色 | 无色 | |
3 | 0.25mL | 浅黄色 | 蓝色 | |
4 | 0.30mL | 无色 | 蓝色 |
(1)取实验2后的溶液,进行如下实验:
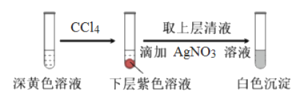
经检验,上述白色沉淀是AgCl。写出加入0.20mLNaClO3后,溶液中ClO3-和I-发生反应的离子方程式____________。
(2)查阅资料:一定条件下,I-和I2都可以被氧化成IO3-。
作出假设:NaClO3溶液用量增加导致溶液褪色的原因是过量的NaClO3溶液与(1)中的反应产物继续反应,同时生成Cl2,反应的离子方程式是______________________。
进行实验:取少量实验4中的无色溶液进行以下实验,进一步佐证其中含有IO3-。其中试剂X可以是_________(填字母序号)。
a.碘水 b.KMnO4溶液 c.NaHSO3溶液
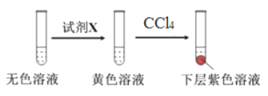
获得结论:NaClO3溶液用量增加导致溶液褪色。
(3)小组同学继续实验,通过改变实验4中硫酸溶液的用量,获得如下实验结果:
编号 | 6.0mol·L-1H2SO4溶液用量 | 试管中溶液颜色 | 淀粉KI试纸颜色 |
5 | 0.25mL | 浅黄色 | 无色 |
6 | 0.85mL | 无色 | 蓝色 |
①对比实验4和5,可以获得的结论是______________________。
②实验6中ClO3-和I-反应的离子方程式是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫化氢大量存在于天然气及液化石油气中,近年来发现![]() 可用于制取氢气、合成硫醇等。回答下列问题:
可用于制取氢气、合成硫醇等。回答下列问题:
(1)D.Berk等学者设计的用FeS催化分解![]() 包括下列反应:
包括下列反应:
Ⅰ.![]()
Ⅱ.![]()
Ⅲ.![]()
①![]() =____________(用
=____________(用![]() 表示)。
表示)。
②已知单质硫气态时以![]() 形式存在(结构为S=S)。键能E(H-S)=339
形式存在(结构为S=S)。键能E(H-S)=339![]() 、E(H-H)=436
、E(H-H)=436![]() 、E(S=S)=225
、E(S=S)=225![]() ,则
,则![]() =____________
=____________![]() 。
。
③![]() 是离子化合物,Fe显+2价,
是离子化合物,Fe显+2价,![]() 的电子式为______________。
的电子式为______________。
(2)银器长期露置在含![]() 的空气中表面会生成
的空气中表面会生成![]() 而变黑,该反应的氧化剂为________;将表面变黑的银器放在盛有食盐水的铝制容器中煮沸,表面重新变为光亮,正极发生的电极反应为________。
而变黑,该反应的氧化剂为________;将表面变黑的银器放在盛有食盐水的铝制容器中煮沸,表面重新变为光亮,正极发生的电极反应为________。
(3)实验室用粗锌制取氢气时常含有少量的![]() ,可用酸性
,可用酸性![]() 溶液(
溶液(![]() 被还原为
被还原为![]() )将
)将![]() 氧化为S而除去,该反应的离子方程式为_______。
氧化为S而除去,该反应的离子方程式为_______。
(4)![]() 与
与![]() 合成硫醇
合成硫醇![]() 的反应
的反应![]() 在不同温度及不同物质的量之比时
在不同温度及不同物质的量之比时![]() 的平衡转化率如图所示:
的平衡转化率如图所示:
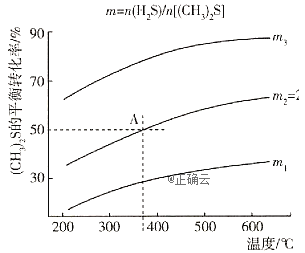
①该反应的![]() ______0(填“>”或“<");
______0(填“>”或“<");![]() _________
_________![]() (填“>”或“<”)。
(填“>”或“<”)。
②在2L密闭容器中充入0.2mol![]() 和0.1mol
和0.1mol![]() ,在A点达到平衡时,A点对应温度下反应的平衡常数为K=_________。
,在A点达到平衡时,A点对应温度下反应的平衡常数为K=_________。
③为提高![]() 的平衡转化率,除改变温度及投料比(m)外,还可采取的措施是_____
的平衡转化率,除改变温度及投料比(m)外,还可采取的措施是_____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:3H2(g)+N2(g)2NH3(g)△H=-92kJ/mol,在催化剂存在时反应过程中的能量变化如图所示。下列叙述正确的是
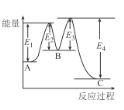
A.△H=E2-E1+E3-E4
B.加入催化剂后反应经过两步完成,其中第一步反应决定总反应速率
C.加入催化剂,△H、反应速率均发生改变
D.向密闭容器中充入3 mol H2和1molN2,发生上述反应,达到平衡时,反应放出92 kJ热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向温度为300℃的2 L密闭容器中充入2 mol SO2和1 mol O2,发生反应2SO2 (g)+ O2 (g) ![]() 2SO3(g)△H<0,体系达到平衡状态后SO2的浓度为0.1 mol/L,下列说法错误的是
2SO3(g)△H<0,体系达到平衡状态后SO2的浓度为0.1 mol/L,下列说法错误的是
A.该温度下,反应的平衡常数K =1620
B.SO2和O2的平衡转化率相等
C.平衡后保持温度和容器体积不变,再充入SO3(g),平衡常数不变
D.若不再向容器中加入任何物质,仅改变条件不可能使SO2的浓度达到1 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上将石灰石和硫煤混合使用,称之为“固硫”,其反应原理为:2CaCO3(s)+2SO2(g)+O2(g)![]() 2CaSO4(s)+2CO2(g) △H1=akJ·mol-1。
2CaSO4(s)+2CO2(g) △H1=akJ·mol-1。
已知:CaO(s)+CO2(g)![]() CaCO3(s) △H2=bkJ·mol-1;
CaCO3(s) △H2=bkJ·mol-1;
2SO2(g)+O2(g)![]() 2SO3(g) △H3=ckJ·mol-1。
2SO3(g) △H3=ckJ·mol-1。
请回答下列问题:
(1)CaSO4(s)![]() CaO(s)+SO3(g)△H=___kJ·mol-1(用a、b、c表示)。
CaO(s)+SO3(g)△H=___kJ·mol-1(用a、b、c表示)。
(2)T1℃时,向某恒容密闭容器中通入一定量的CO2和足量CaO发生反应:CaO(s)+CO2(g)![]() CaCO3(s),CO2的浓度随时间变化如图所示:
CaCO3(s),CO2的浓度随时间变化如图所示:
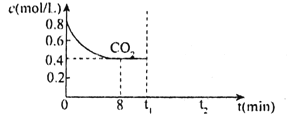
①0~8min,v(CO2)=___。
②t1min时,若保持其他条件不变,压缩容器体积至原来的![]() ,t2min重新达到平衡,请在图中画出CO2的浓度自条件改变至新平衡的变化曲线___。
,t2min重新达到平衡,请在图中画出CO2的浓度自条件改变至新平衡的变化曲线___。
(3)T2℃时,向某密闭容器中通入2molSO2和1molO2发生反应:2SO2(g)+O2(g)![]() 2SO3(g) △H3=ckJ·mol-1。
2SO3(g) △H3=ckJ·mol-1。
①若该容器为恒压密闭容器,下列选项可判断反应已达平衡状态的是___。
A.混合气体的密度不再改变
B混合气体的压强不再改变
C.相同时间内,每断裂0.1molO=O键,同时生成0.2molSO3
D.混合气体的平均相对分子质量不再改变
②若该容器为2L的恒容密闭容器,达平衡时SO3的体积分数为40%,则O2的转化率为___,T2℃时该反应的平衡常数K=___。
③反应达到②中的平衡状态后,保持反应温度和O2的浓度不变,增大容器体积,则平衡将___(填“正向”、“逆向”或“不“)移动,原因为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中能大量共存的是( )
A.无色透明的溶液中: Fe3+、Mg2+、SCN 、Cl
B.![]() =1×10-12的溶液中:K+、Na+、CO32、NO3
=1×10-12的溶液中:K+、Na+、CO32、NO3
C.![]() 的溶液中: K+、NH4+、MnO4、SO42-
的溶液中: K+、NH4+、MnO4、SO42-
D.能使甲基橙变红的溶液中: Na+、NH4+、SO42-、HCO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】垃圾分类正在全国逐渐推广,垃圾资源化是可持续、绿色发展的重要途径。由金属废料(主要含铁、铜和它们的氧化物)制得碱式碳酸铜和摩尔盐[(NH4)2SO4·FeSO4·xH2O]的工艺流程如图所示:

已知:Ksp[Fe(OH)3]=1×10-38,Ksp[Cu(OH)2]=2.2×10-20,一般认为某离子浓度小于或等于10-5mol/L时,该离子转化或去除完全。
请回答下列问题:
(1)热纯碱的作用是__,H2O2的电子式为__。
(2)调pH步骤可选用的试剂为__。
A.CuO B.Cu(OH)2 C.Fe2O3 D.Fe(OH)3
(3)若所得溶液中c(Cu2+)=0.22mol·L-1,则需要调节的pH范围是__。
(4)溶液1经过加热、蒸发至__时,自然冷却即可得到晶体,然后抽滤,用酒精洗涤晶体,酒精洗涤的目的是__。
(5)写出该流程中生成碱式碳酸铜的离子方程式__。
(6)取3.92g摩尔盐产品,在隔绝空气的条件下加热至135°C时完全失去结晶水,此时固体质量为2.84g,则该摩尔盐结晶水个数x=__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com