
| A. | NH3$→_{催化剂}^{O_{2}}$NO$\stackrel{O_{2}•H_{2}O}{→}$HNO3 | |
| B. | 浓缩海水$\stackrel{CI_{2}}{→}$Br2$\stackrel{鼓入热空气}{→}$Br2(粗产品)$\stackrel{精制}{→}$Br2 | |
| C. | MnO2$→_{加热}^{浓HCI}$Cl2$\stackrel{Ca(OH)_{2}}{→}$漂白粉 | |
| D. | 石油$\stackrel{裂解}{→}$乙烯$→_{加热}^{催化剂}$聚乙烯 |
分析 A.硝酸工业是利用氨气的催化氧化生成一氧化氮,一氧化氮被氧气氧化为二氧化氮,二氧化氮和水发生反应生成硝酸;
B.海水提溴是先通入足量氯气氧化溴离子为溴单质,然后将溴单质还原为溴化氢,再通入适量氯气氧化溴离子为溴单质,最后萃取;
C.工业制漂白粉先是电解饱和食盐水得到氯气,用氯气和石灰乳反应得到漂白粉;
D.石油通过裂解可直接得到乙烯,乙烯发生加聚反应生成聚乙烯.
解答 解:A.硝酸工业是利用氨气的催化氧化生成一氧化氮,一氧化氮被氧气氧化为二氧化氮,二氧化氮和水发生反应生成硝酸,即NH3$→_{催化剂}^{O_{2}}$NO$\stackrel{O_{2}•H_{2}O}{→}$HNO3,故A正确;
B.提溴的工艺是在预先浓缩并酸化的海水中,通入足量氯气发生氧化反应,然后使生成的溴与吸收剂SO2反应转化为氢溴酸以达到富集溴元素的目的发生还原反应,再通入适量氯气氧化溴离子为溴单质,即浓缩水$\stackrel{CI_{2}}{→}$Br2$\stackrel{鼓入热空气}{→}$Br2(粗产品)$\stackrel{精制}{→}$Br2,故B正确;
C.工业制漂白粉先是电解饱和食盐水得到氯气,用氯气和石灰乳反应得到漂白粉,不是采用二氧化锰和浓盐酸反应生成氯气,故C错误;
D.石油通过裂解可直接得到乙烯,乙烯发生加聚反应生成聚乙烯,即石油$\stackrel{裂解}{→}$乙烯$→_{加热}^{催化剂}$聚乙烯,故D正确.
故选C.
点评 本题考查了工业制备的过程分析,反应原理的应用,侧重于化学与生活、生产的考查,有利于培养学生的良好的科学素养,提高学习的积极性,注意海水提溴的原理,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 白磷、硅 | B. | 碳化硅、硫酸钠 | C. | 水晶、金刚石 | D. | 碘、汞 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
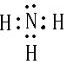 ,该氢化物中含有的化学键是极性共价键.
,该氢化物中含有的化学键是极性共价键.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+、CH3COO-、Ca2+、Cl- | B. | Fe3+、Ag+、SO42-、NO3- | ||
| C. | Cu2+、H+、S2-、NO3- | D. | C6H5OH、Fe3+、K+、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 溶液中一定有K+、Br-、CO32-、AlO2- | |
| B. | 溶液中一定没有Mg2+、Cu2+、Cl-、NH4+ | |
| C. | 不能确定溶液中是否有K+、SO42-、Cl- | |
| D. | 往第3份溶液中滴加BaCl2可确认是否有SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
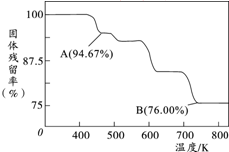 铬元素及其化合物在生产、生活中具有广泛的用途.
铬元素及其化合物在生产、生活中具有广泛的用途.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X、M两元素最简单氢化物的稳定性:X<M | |
| B. | Z、W、M的单质均能与稀硫酸反应制取氧气,且反应剧烈程度依次减弱 | |
| C. | Y的最高价含氧酸的化学式为H2YO2 | |
| D. | W和M的氧化物均可作耐高温材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验组号 | ① | ② | ③ | ④ |
| 碳化物(g) | 6.2 | 9.3 | 15.5 | 21.7 |
| 水(mL) | 18 | 18 | 18 | 18 |
| 气体(L,标准状况) | 3.36 | 5.04 | 8.4左右 | 8.4左右 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com