
【题目】钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢铁占世界钢铁年产量的四分之一。
请回答钢铁在腐蚀、防护过程中的有关问题。
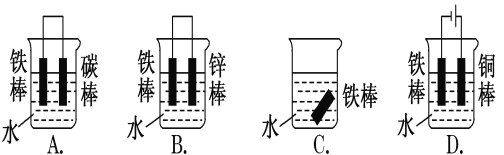
(1)下列哪些装置不能防止铁棒被腐蚀________________;
(2)实际生产可在铁件的表面镀铜防止铁被腐蚀.装置示意图如图.请回答:
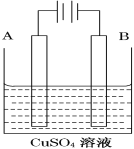
①B电极对应的金属是________(写元素名称),
A电极的电极反应式是___________________。
②镀层破损后,镀铜铁比镀锌铁更容易被腐蚀,请简要说明原因_____________________。
 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
【题目】硫的化合物在工业上有广泛的应用,因此研究硫的化合物制备有着重要的意义.某同学拟采用下图装置(实验前已除尽装置内的空气)来制取焦亚硫酸钠(Na2S2O5).已知装置图l—II中有Na2S2O5晶体析出,发生的反应为Na2SO3+SO2=Na2S2O5
(l)装置I是用亚硫酸钠固体和浓硫酸制备二氧化硫气体,该装置中反应的化学方程式为______________;如果想控制反应速度,图2中可选用的发生装置是_______(填写字母).

(2)装置Ⅱ中有Na2S2O5晶体析出,要获得已析出的晶体可采取的分离方法是________________
(3)装置III用于处理尾气,可选用的最佳试剂是______________(填序号).
a、饱和食盐水 b、NaOH溶液 c、浓硫酸 d、饱和NaHCO3溶液
(4)Na2S2O5与稀硫酸反应放出SO2,其离子方程式为___________________
(5)工业制备得到产品Na2S2O5中含有杂质碳酸钠,检验产品中含有碳酸钠杂质所需试剂是___________(填编号)(已知Na2S2O5溶于水即生成NaHSO3)
①酸性高锰酸钾 ②品红溶液 ③澄清石灰水
④饱和碳酸氢钠溶液 ⑤NaOH ⑥稀硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】DNA是控制遗传性状的遗传物质,在水稻的细胞中它分布在( )
A. 细胞核、内质网 B. 细胞核、核糖体
C. 细胞核、细胞质基质 D. 细胞核、线粒体、叶绿体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用右图装置完成下表所列的四个实验,不能达到实验目的是
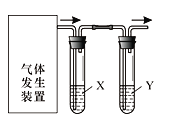
选项 | 实验目的 | 试剂X | 试剂Y |
A | 验证C2H5OH与浓H2SO4加热至170℃制得的乙烯的性质 | NaOH溶液 | Br2水 |
B | 检验FeSO4受热分解产生的气体中有SO3和SO2 | BaCl2溶液 | 品红溶液 |
C | 验证电石与饱和食盐水反应生成的乙炔的性质 | CuSO4溶液 | KMnO4溶液 |
D | 验证氧化性:Cl2>Br2>I2 | NaBr溶液 | KI溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人的红细胞必须生活在一定浓度的溶液中,医生给脱水的病人注射用的都是渗透压与血浆一致的浓度为0.9%的生理盐水。如果将红细胞放入蒸馏水中,红细胞就会因吸水过多而胀破;放入浓盐水中则会因失水过多而皱缩,从而失去运输氧的功能,这说明( )
A. 水分子容易进出细胞
B. 无机盐离子容易进出细胞
C. 红细胞的特性造成的
D. 无机盐对维持细胞的形态和功能具有重要作用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学反应属于吸热反应的是
A. 浓H2SO4溶于水 B. 生石灰溶于水
C. 镁与稀盐酸反应 D. NH4Cl固体与Ba(OH)2·8H2O混合
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小儿患佝偻病,发烧时就会抽搐,根据所学知识,建议他平时要补充
A. 新鲜水果和蔬菜 B. 钙片和维生素D
C. 谷物种皮和胡萝卜 D. 蛋白质和糖类
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】砷的常见酸性氧化物有As2O3和As2O5,根据图中信息回答下列问题:
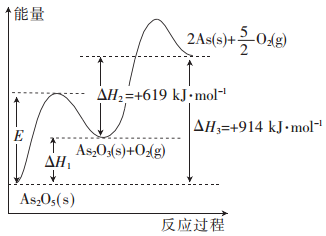
(1)As2O5分解生成As2O3和O2的反应中,加入催化剂,E__________(填“增大”、“减小”或 “不变”,下同),△H1_________。
(2)As2O3分解生成As和O2的热化学方程式为____________________。
(3)As2O3和O2反应生成As2O5的热化学方程式为_____________________。
(4)若1 mol As2O5分解生成0.4 mol As2O3和1.2 mol As,则该分解过程中,需吸收的总能量为_________kJ。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com