
A.2NaCl(熔融) 2Na+Cl2↑ 2Na+Cl2↑ | B.Al2O3+3H2 2Al+3H2O 2Al+3H2O |
C.Fe3O4+4CO 3Fe+4CO2↑ 3Fe+4CO2↑ | D.2HgO 2Hg+O2↑ 2Hg+O2↑ |
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用有机溶剂可萃取海水中的溴、碘 |
| B.海水中含有碘元素,只需将海水中的碘升华就可以得到碘单质 |
| C.从海水中可以得到NaCl,NaCl可以是制造化肥的原料 |
| D.常用电解氯化钠和氯化镁的水溶液来制得钠和镁 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
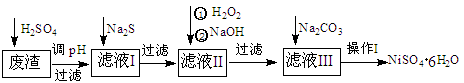
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.金属在自然界的存在形式 | B.金属熔点的高低 |
| C.金属离子得电子的能力 | D.金属元素在地壳中的含量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.熔融的MgO不导电 | B.MgO分子间作用力很大 |
| C.MgO熔点高 | D.MgO属原子晶体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.②③ | B.②④ | C.③④ | D.①③ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com