
往一个容积为5L的密闭容器中,通入2molN2和3molH2,在一定条件下,发生反应 N2+3H2 2NH3,2 min后测得容器中生成了1mol NH3,试求:
2NH3,2 min后测得容器中生成了1mol NH3,试求:
(1)2 min时,N2的物质的量 ;
(2) 2 min时,H2的物质的量浓度 ;
(3)2 min时,H2的转化率 ;
(4)2min内,N2的平均反应速率 ;
 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案科目:高中化学 来源: 题型:
化学与人类生产,生活密切相关。下列有关说法不正确的是
A.“海水淡化”可以解决“淡水供应危机”,向海水中加入净水剂明矾可以使海水淡化
B.福尔马林可浸制标本,利用了其使蛋白质变性的性质
C.医用酒精使用淀粉类植物发酵经蒸馏制成,浓度通常为75%
D.绚丽缤纷的烟花中添加了含钾,钙,钠,铜等金属元素化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
对于常温下pH为1的硝酸溶液,下列叙述正确的是( )
A.该溶液1 mL稀释至100 mL后,pH等于3
B.向该溶液中加入pH为13的氢氧化钡溶液恰好完全中和
C.该溶液中硝酸电离出的c(H+)与水电离出的c(H+)之比值为10-12
D.该溶液中水电离出的c(H+)是pH为3的硝酸中水电离出的c(H+)的100倍
查看答案和解析>>
科目:高中化学 来源: 题型:
 在5L的密闭容器中进行下述反应4NH3(g)+5O2(g)
在5L的密闭容器中进行下述反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g) 30S内,NO增加了0.3mol,则在30S内,该反应的平均反应速率正确的是( )
4NO(g)+6H2O(g) 30S内,NO增加了0.3mol,则在30S内,该反应的平均反应速率正确的是( )
A.V(O2 )=0.01mol·L-1·s-1 B. V(NO )=0.08mol·L-1·s-1
C. V(H2O)=0.01mol·L-1·s-1 D. V(NH3)=0.002mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
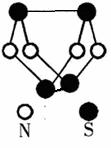
现代无机化学对硫-氮化合物的研究是最为活跃的领域之一。下图是已经合成的最著名的硫-氮化合物的分子结构。下列说法正确的是( )
A.该物质与S2N 2互为同素异形体
B.该物质的分子中既有极性键又有非极性键
C.该物质可能是离子化合物
D.该物质的一个分子中含有9个N—S键
查看答案和解析>>
科目:高中化学 来源: 题型:
已知C(石墨,s) = C(金刚石,s) △H>0,
P(白磷,s) = P(红磷,s) △H<0。根据上述信息推论正确的是( )
A.前者为放热反应 B.红磷的能量比白磷低
C.红磷比金刚石稳定 D.上述变化都为物理变化
查看答案和解析>>
科目:高中化学 来源: 题型:
对于反应M + N = P,如果温度每升高10℃,化学反应速率增加到3倍,在20℃时完成该反应的30%需要81 min,若将温度升高到40℃,完成该反应的30%需要时间为( )
A.9 min B.27 min C.13.5 min D.3 min
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)对于下列反应:2SO2(g) + O2(g) 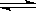 2SO3(g) , 如果2min内SO2的浓度由6 mol/L下降为2 mol/L,用SO2浓度变化来表示的化学反应速率为____________,用O2浓度变化来表示的反应速率为_____________。如果开始时SO2浓度为4mol/L,2min后反应达平衡,若这段时间内v(O2)为0.5mol/(L·min),那么2min时SO2的浓度为 。
2SO3(g) , 如果2min内SO2的浓度由6 mol/L下降为2 mol/L,用SO2浓度变化来表示的化学反应速率为____________,用O2浓度变化来表示的反应速率为_____________。如果开始时SO2浓度为4mol/L,2min后反应达平衡,若这段时间内v(O2)为0.5mol/(L·min),那么2min时SO2的浓度为 。
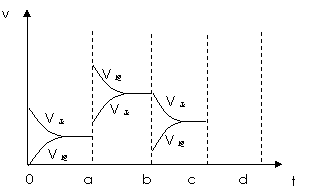
(2)下图表示在密闭容器中反应:2SO2+O2 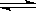 2SO3 △H<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a~b过程中改变的条件可能是 ;b~c过程中改变的条件可能是 ; 若增大压强时,反应速度变化情况画在c~d处。
2SO3 △H<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a~b过程中改变的条件可能是 ;b~c过程中改变的条件可能是 ; 若增大压强时,反应速度变化情况画在c~d处。
 |
(3)以上反应达平衡后,
若此时只将容器的体积扩大为原来的2倍,达新平衡时,容器内温度将降低(容器不与外界进行热交换),则该反应正向为 反应(填“放热”或“吸热”);达新平衡时,容器内混合气体的平均相对分子质量
比原平衡时 (填“增大”、“减小”或“相等”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
合成氨所需氢气可由煤和水反应制得,其中一步反应为
CO(g)+H2O(g) 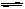 CO2(g)+H2(g) ΔH<0,欲提高CO的转化率可采用的措施是
CO2(g)+H2(g) ΔH<0,欲提高CO的转化率可采用的措施是
① 降低温度 ②增大压强 ③使用催化剂 ④增大CO的浓度 ⑤增大水蒸气的浓度
A.①②③ B.④⑤ C. ①⑤ D.⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com