
某课外活动小组用镁条与盐酸反应制氢气,推算标准状况下1 mol H2的体积.现有下列实验用品:电子天平,100 mL口径较小的测气管(如图),500 mL烧杯、100 mL烧杯、铁架台、单孔橡皮塞(与测气管径相配)、细铜丝、砂纸、镁条、水.
(1)还缺0.6 mol/L的盐酸480 mL,现请你用12 mol/L的浓盐酸进行配制,写出必须增补的实验仪器名称及规格________.
(2)选用上述药品和仪器(包括规格),完成下列实验步骤,直到反应结束.
①取一段镁条,擦去氧化物,称量.
②用细铜丝系住镁条,一端留有握持部分.
③________.
④________.
⑤________.
⑥________.
⑦待镁条全部反应后,放置10 min,调节测气管中水面的高度,使管内外的水面相平齐,读出氢气的体积.
(3)简答下列问题.
①为什么要放置10 min?________.
②为什么测气管内外水面要平齐?________.
③实验时,所处环境不是标准状况,除了测定所用镁条质量、放出氢气的体积外,还应测定哪些数据?________.
④某生做了三次实验,计算结果是:第一次:1 mol H2体积22.530 L;第二次:1 mol H2体积23.700 L;第三次:1 mol H2体积22.470 L;本次实验得出1 moL H2在标准状况下的体积为________.
⑤每次做实验所用的镁条质量为________.
A.0.030 g B.0.200 g C.0.080 g D.0.120 g
|
答案:(1)500 mL容量瓶、胶头滴管、玻璃棒、50 mL量筒; (2)③向测气管中注入少量0.6 mol/L的盐酸(>1.5 mL);④再向测气管中缓缓注入水至满(不能振荡);⑤镁条浸入管口的水中,加单孔塞使铜丝固定;⑥用手指抵住橡皮塞倒转测气管浸入盛有水的500 mL烧杯中(盐酸密度比水大,向下扩散与镁条接触发生反应); (3)①冷却,使管内气温与室温相同;②使管内外气压相等;③室温和室内气压;④(22.530 L+22.470 L)/2=22.500;⑤C 解析:(1)配480 mL溶液,须增补容积为500 mL的容量瓶,所需浓盐酸的体积为25 mL,须增补50 mL的量筒(容量瓶的规格有50 mL、100 mL、250 mL、500 mL、1 000 mL等几种;量筒的规格有10 mL、50 mL、100 mL、500 mL、1 000 mL等几种). (2)要利用测气管和烧杯完成镁与酸的反应,并且用测气管准确收集氢气进行测量,只能用排水集气法,又不能让H2逸漏,所以反应也就在测气管中进行. (3)因为测定的体积不是标准状况下的,①和②问的目的是为了使氢气的温度和压强与室温及室内气压相同,然后根据理想气体状态方程进行换算,得到标准状况下的体积,所以第③问还应测出室温和室内气压,第④问,因为第二次所得数据与第一、三次的相比误差太大,应舍去.第⑤问,要保证Mg能反应完,并且放出的H2全部收集在测气管中,即H2的体积必须小于100 mL,决定了Mg的质量应小于0.107 g(但是又不能太小,否则制得的气体太少,测定的误差较大),6 mol/L的盐酸又应大于1.5 mL,才能使Mg反应完. |
|
本题集实验原理及步骤的设计、仪器及其规格的选择、实验数据的处理、药品用量的确定于一题,并与物理内容综合于一体,题型新颖灵活,是一道考查学生实验技能、思维能力的好题. |


科目:高中化学 来源: 题型:
| ||
| ||
| ||
| ||
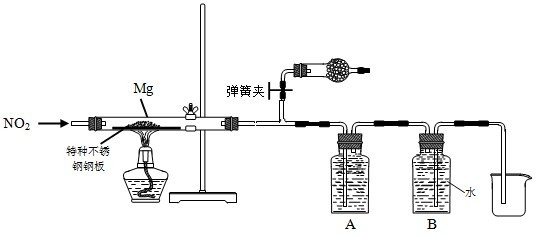
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
实验用品:
仪器:电子天平、砂纸、水槽、100 mL烧杯、铁架台、单孔橡皮塞(玻璃管上带橡胶管和止水夹)、铜丝、30 mL酸式滴定管、100 mL小口径测气管(见下图)。
![]()
药品:镁条、水、15 mol·L-1的浓硫酸。
(1)本实验用0.6 mol·L-1的硫酸进行反应,活动小组共需要480 mL该浓度的硫酸,写出用15 mol·L-1的浓硫酸配制0.6 mol·L-1的硫酸时,还用到的仪器名称和规格____________、____________、____________;需要15 mol·L-1的浓硫酸____________mL。
(2)选用上述仪器的药品进行实验,补写下列实验步骤:
①取一段镁条,擦去氧化膜,称量;
②用细铜丝包裹镁条,铜丝的另一端插在单孔橡皮塞(玻璃管上带橡胶管和止水夹)上;
③_____________________________________________________________;
④_____________________________________________________________;
⑤_____________________________________________________________;
⑥待镁条全部反应后,放置一段时间,调节测气管中水面高度,使管中水面与水槽中水面相平,读出氢气体积。
(3)问题讨论:
①在标准状况下,其他操作都正常,为了保证实验成功,取用的镁条质量应小于_________________g,所用的稀硫酸应大于_________________mL。
②在标准状况下,某学生进行了5次实验,将实验数据通过计算,结果如下:
实验序号 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
H2的体积(L·mol-1) | 23.45 | 22.41 | 22.38 | 22.39 | 22.42 |
则通过实验验证,标准状况下,1 mol H2的体积为____________L。
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
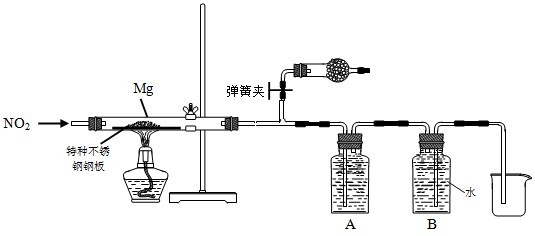
查看答案和解析>>
科目:高中化学 来源:2013年北京市丰台区高考化学二模试卷(解析版) 题型:填空题
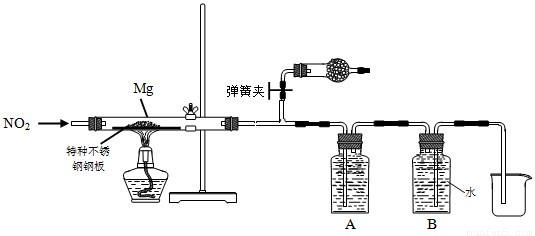
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com