
科目:高中化学 来源: 题型:
下列鉴别实验中,所选试剂不合理的是
A.用水鉴别乙醇和苯 B.用碳酸氢钠溶液鉴别乙酸和乙醇
C.用新制的氢氧化铜鉴别葡萄糖和蔗糖 D.用高锰酸钾酸性溶液鉴别甲苯和己烯
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验能达到预期目的是( )
①用乙醇和浓硫酸除去乙酸乙酯中的少量乙酸; ②用饱和NaHCO3溶液除去CO2中的少量HCl
③用醋和澄清石灰水验证蛋壳中含有碳酸盐④在试管中煮沸液体时加入一小块瓷片可以防止飞溅;
⑤用盐酸酸化的氯化钡溶液检验溶液中的SO42-.
A.②③④ B.②③⑤ C.②③④⑤ D.①②③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
.将SO2分别通入下列4种溶液中,有关说法正确的是
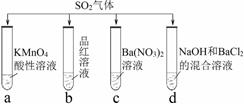
A.试管a中实验可以证明SO2具有漂白性 B.试管b中溶液褪色,说明SO2具有强氧化性
C.试管c中能产生白色沉淀,说明SO2具有还原性
D.试管d中能产生白色沉淀,该沉淀完全溶于稀硝酸
查看答案和解析>>
科目:高中化学 来源: 题型:
影响化学反应速率的因素很多,某校化学小组用实验的方法进行探究。
实验一:他们只利用Cu、Fe、Mg和不同浓度的硫酸(0.5 mol·L-1、2 mol·L-1、18.4 mol·L-1)设计实验方案来研究影响反应速率的因素。
甲同学的实验报告如下表:
| 实验步骤 | 现象 | 结论 |
| ①分别取等体积的2 mol·L-1的硫酸于试管中 ②____________ | 反应速率Mg>Fe,Cu不反应 | 金属的性质越活泼,反应速率越快 |

(1)甲同学表中实验步骤②为____________________________。
(2)甲同学的实验目的是____________________________________________________
________________________________________________________________________;
要得出正确的实验结论,还需控制的实验条件是____________。乙同学为了更精确地研究浓度对反应速率的影响,利用如图所示装置进行定量实验。
(3)乙同学在实验中应该测定的数据是
________________________________________________________________________
________________________________________________________________________。
(4)乙同学完成该实验应选用的实验药品是____________
________________________________________________________________________,
该实验中不选用某浓度的硫酸,理由是______________________________________
________________________________________________________________________。
实验二:已知 2KMnO4+5H2C2O4+3H2SO4===K2SO4+2MnSO4+8H2O+10CO2↑,在高锰酸钾酸性溶液和草酸溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快。
(5)针对上述实验现象,丙同学认为KMnO4与H2C2O4反应放热,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你猜想还可能是______________的影响。
(6)若用实验证明你的猜想,除高锰酸钾酸性溶液、草酸溶液外,还需要选择的试剂最合理的是________(填字母)。
A.硫酸钾 B.硫酸锰
C.二氯化锰 D.水
查看答案和解析>>
科目:高中化学 来源: 题型:
2SO2(g)+O2(g)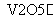 2SO3(g)是制备硫酸的重要反应。下列叙述正确的是( )
2SO3(g)是制备硫酸的重要反应。下列叙述正确的是( )
A.催化剂V2O5不改变该反应的逆反应速率
B.增大反应体系的压强,反应速率一定增大
C.该反应是放热反应,降低温度将缩短反应达到平衡的时间
D.在t1、t2时刻,SO3(g)的浓度分别是c1、c2,则时间间隔t1~t2内,SO3(g)生成的平均速率为v=
查看答案和解析>>
科目:高中化学 来源: 题型:
运用化学反应原理研究卤族元素的性质具有重要意义。
(1)下列关于氯水的叙述正确的是________(填写字母)。
a.氯水中存在两种电离平衡
b.向氯水中通入SO2,其漂白性增强
c.向氯水中通入氯气,c(H+)/c(ClO-)减小
d.加水稀释氯水,溶液中的所有离子浓度均减小
e.加水稀释氯水,水的电离平衡向正反应方向移动
f.向氯水中加入少量固体NaOH,可能有c(Na+)=c(Cl-)+c(ClO-)
(2)常温下,已知25 ℃时有关弱酸的电离平衡常数:
| 弱酸化学式 | HClO | H2CO3 |
| 电离平衡常数 | 4.7×10-8 | K1=4.3×10-7 K2=5.6×10-11 |
写出84消毒液露置在空气中发生反应的离子方程式
________________________________________________________________________
________________________________________________________________________。
(3)电解饱和食盐水可得到溶质为M的碱溶液,常温下将浓度为c1的M溶液与0.1 mol·L-1的一元酸HA等体积混合,所得溶液pH=7,则c1________0.1 mol·L-1(填“≥”、“=”或 “≤”),溶液中离子浓度的大小关系为______________________________。若将上述“0.1 mol·L-1的一元酸HA”改为“pH=1的一元酸HA”,所得溶液pH仍为7,则c1________0.1 mol·L-1。
(4)牙釉质对牙齿起着保护作用,其主要成分为羟基磷灰石,研究证实氟磷灰石比它更能抵抗酸的侵蚀,故含氟牙膏已使全世界千百万人较少龋齿,请写出羟基磷灰石的溶度积常数表达式Ksp=____________,氟离子与之反应转化的离子方程式为
________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com