
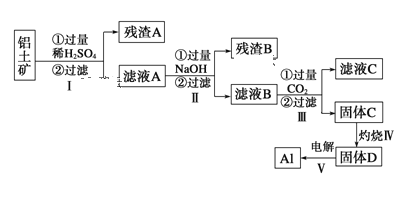
【题目】(铝用途广泛,用铝土矿(主要成分为Al2O3·nH2O、少量SiO2和Fe2O3)制取Al有如下途径:
(1)滤液A加过量NaOH离子方程式表示为______________________________
(2)灼烧时盛放药品的仪器名称是_______
(3)步骤Ⅳ中发生反应的化学方程式是___________________________________
(4)步骤Ⅲ中生成固体C的离子反应方程式为_____________________________
(5)取滤液B 100mL,加入1 mol/L盐酸200 mL,沉淀量达到最大且质量为11.7g,则滤液B中c(AlO2-)____mol/L,c(Na+)____6.5 mol/L (填“大于”、“小于”或“等于”)
【答案】H++OH-=H2O、4OH-+Al3+=AlO2-+2H2O、Fe3++3OH- = Fe(OH)3↓ 坩埚 2Al(OH)3![]() Al2O3+3H2O AlO2-+CO2+2H2O =Al(OH)3↓+HCO3- 1.5 大于
Al2O3+3H2O AlO2-+CO2+2H2O =Al(OH)3↓+HCO3- 1.5 大于
【解析】
铝土矿溶解在过量稀硫酸中,过滤后得到的滤渣是SiO2,滤液为Al2(SO4)3、H2SO4、Fe2(SO4)3的混合液。因Al3+、Fe3+能水解产生具有吸附作用的Al(OH)3、Fe(OH)3胶体,具有净水作用。向Al2(SO4)3、H2SO4、Fe2(SO4)3的混合液中加入过量NaOH时,Al2(SO4)3转化为NaAlO2,Fe2(SO4)3转化为Fe(OH)3,经过滤后得到滤渣Fe(OH)3。滤液B中含有NaAlO2,向滤液B中通入过量CO2时,生成Al(OH)3和NaHCO3,经过滤后得到固体C[Al(OH)3]和含有NaHCO3、Na2SO4的滤液C。
(1)根据以上分析,滤液A中含有H2SO4、Al2(SO4)3、Fe(SO4)3,加入过量NaOH,故反应的离子方程式为H++OH-=H2O、4OH-+Al3+═AlO2-+2H2O、Fe3++4OH-═Fe(OH)3↓;故答案为:H++OH-=H2O、4OH-+Al3+═AlO2-+2H2O、Fe3++4OH-═Fe(OH)3↓;
(2)根据加热溶液一般在蒸发皿里进行,而灼烧固体一般在坩埚中进行,故答案:坩埚;
(3)根据以上分析,固体C为氢氧化铝,所以步骤Ⅳ中发生反应的化学方程式2Al(OH)3 ![]() Al2O3+3H2O;
Al2O3+3H2O;
(4)步骤Ⅲ中生成固体C的反应是向滤液B中通入二氧化碳气体,根据以上分析,滤液B中含有NaAlO2,故反应的离子方程式:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3-;
(5)根据以上分析滤液B中含有硫酸钠、偏铝酸钠、过量的氢氧化钠,向滤液中加入1mol/L盐酸200mL,沉淀量达到最大且质量为11.7g为Al(OH)3的质量,则根据铝原子守恒,c(AlO2-)= ![]() =
= 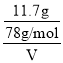 =1.5molL-1。最后所得的溶液中溶质为硫酸钠、氯化钠,根据钠离子守恒有n(NaOH)=n(NaCl)+2(Na2SO4),根据氯离子与硫酸根守恒有n(NaCl)=n(HCl)=0.2L×1mol/L=0.2mol,n(Na2SO4)=n(H2SO4)>3n(Al2(SO4)3)=3×
=1.5molL-1。最后所得的溶液中溶质为硫酸钠、氯化钠,根据钠离子守恒有n(NaOH)=n(NaCl)+2(Na2SO4),根据氯离子与硫酸根守恒有n(NaCl)=n(HCl)=0.2L×1mol/L=0.2mol,n(Na2SO4)=n(H2SO4)>3n(Al2(SO4)3)=3×![]() mol=0.45mol,故n(NaOH)=n(NaCl)+2(Na2SO4)>0.2mol+2×0.45mol=1.1mol,故c(Na+)>
mol=0.45mol,故n(NaOH)=n(NaCl)+2(Na2SO4)>0.2mol+2×0.45mol=1.1mol,故c(Na+)>![]() =11mol/L,故答案:1.5;>。
=11mol/L,故答案:1.5;>。


 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:
【题目】中科院某课题组将二氧化锰和生物质置于一个由滤纸制成的折纸通道内形成电池(如图所示),该电池可将可乐(pH=2.5)中的葡萄糖作为燃料获得能量。下列说法中正确的是( )
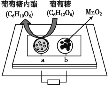
A. a极为正极
B. 随着反应不断进行,负极区的pH不断增大
C. b极电极反应式为MnO2+2H2O+2e-=Mn2++4OH-
D. 消耗0.01mol葡萄糖,电路中转移0.02mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学知识,回答下列问题:
(1)现有下列物质;①KCl晶体②液态HCl③CO2 ④汞⑤CaCO3固体⑥稀硫酸⑦酒精C2H5OH ⑧熔融的NaCl ⑨浓氨水,其中属于电解质的是(填序号,下同)___________;属于非电解质的是____________;能导电的有__________。
(2)已知:2Fe3++2I===2Fe2++I2,2Fe2++Br2===2Fe3++2Br。在含有 FeI2和 FeBr2的溶液中通入少量 Cl2,则最先被氧化的离子是_____,I、Br、Fe2+还原性由强到弱的顺序为:___________。
(3)实验室里盛装NaOH溶液试剂瓶用橡皮塞或软木塞,而不用玻璃塞。用化学方程式解释:_________________________________________________
(4) 0.3mol氨气和0.4mol二氧化碳的质量之比___________,所含分子数之比______________,所含原子数之比____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘被称为“智力元素”,科学合理地补充碘可防治碘缺乏病,KI、KIO3曾先后用于加碘盐中。KI还可用于分析试剂、感光材料、制药等,其制备原理如下:
反应I : 3I2+ 6KOH== KIO3 +5KI+ 3H2O
反应II: 3H2S+KIO3=3S↓+KI+ 3H2O
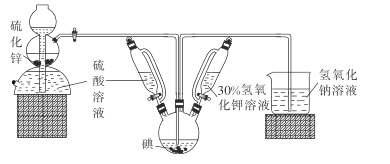
请回答有关问题。
(1)启普发生器中发生反应的化学方程式为_______。装置中盛装30%氢氧化钾溶液的仪器名称是_________。
(2)关闭启普发生器活塞,先滴入30%的KOH溶液.待观察到三颈烧瓶中溶液颜色由棕黄色变为______(填现象) ,停止滴人KOH溶液;然后______(填操作),待三颈烧瓶和烧杯中产生气泡的速率接近相等时停止通气。
(3)滴入硫酸溶液,并对三颈烧瓶中的溶液进行水浴加热,其目的是_____________。
(4)把三颈烧瓶中的溶液倒入烧杯中,加入碳酸钡,在过滤器中过滤,过滤得到的沉淀中除含有过量碳酸钡外,还含有硫酸钡和___________(填名称)。合并滤液和洗涤液,蒸发至析出结晶,干燥得成品。
(5)实验室模拟工业制备KIO3流程如下:
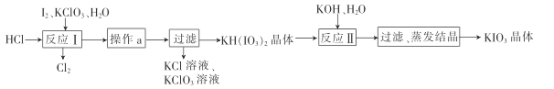
几种物质的溶解度见下表:
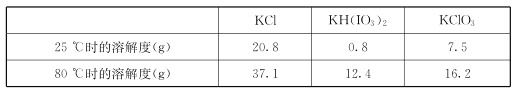
①由上表数据分析可知,“操作a”为__________________。
②用惰性电极电解KI溶液也能制备KIO3,与电解法相比,上述流程制备KIO3的缺点是____________。
(6)某同学测定.上述流程生产的KIO3样品的纯度。
取1.00 g样品溶于蒸馏水中并用硫酸酸化,再加入过量的KI和少量的淀粉溶液,逐滴滴加2.0 mol●L-1 Na2S2O3 溶液,恰好完全反应时共消耗12. 60 mL Na2S2O3溶液。该样品中KIO3的质量分数为_______(已知反应:I2+2Na2S2O3=2NaI+Na2S4O6)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组设计了下列装置,验证二氧化碳跟过氧化钠反应时需要与水接触。

(装置分析)
(1)装置①中反应的离子方程式是____________________________。
(2)装置②中的试剂是________(填序号)。
a.饱和NaHCO3溶液 b.饱和Na2CO3溶液 c.浓H2SO4
(3)装置③中的试剂是__________。
(进行实验)
步骤1:打开弹簧夹K2,关闭K1,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
步骤2:打开弹簧夹K1,关闭K2,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
(4)步骤1和步骤2中,a处带火星的木条产生的实验现象分别是_____________。
(5)过氧化钠跟二氧化碳反应的化学方程式是______________________。
(实验反思)
(6)有同学提出质疑:“上述实验不足以证明有水存在时过氧化钠跟二氧化碳发生了化学反应。”其理由是______。
(7)需要补充的实验操作是:取⑤中反应后的少量固体,______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃A 0.2 mol在氧气中充分燃烧后,生成化合物B、C各1.2 mol,试完成下列问题:
(1)烃A的分子式为____。
(2)若烃A不能使溴水褪色,但在一定条件下,能与氯气发生取代反应,其一氯代物只有一种,则此烃A的结构简式为_____。
(3)若烃A能使溴水褪色,在催化剂作用下,与H2加成,其加成产物经测定分子中含有4个甲基,烃A所有可能的结构简式分别为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,甲、乙、丙、丁四个烧杯中分别盛有100mL蒸馏水,然后分别放入等物质的量的Na、Na2O、Na2O2、NaOH,待固体完全溶解,则四个烧杯中溶液的质量分数的大小顺序为( )
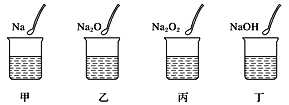
A.甲<乙<丙<丁B.丁<甲<乙=丙C.甲=丁<乙=丙D.丁<甲<乙<丙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:

(1)从实验装置上看,图中尚缺少的一种玻璃仪器是 。
(2)烧杯间填满碎纸条的作用是 。
(3)大烧杯上如不盖硬纸板,求得的中和热数值 (填“偏大、偏小、无影响”)
(4)如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等、不相等”),所求中和热 (填“相等、不相等”),简述理由
(5)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会 ;(填“偏大”、“偏小”、“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化亚硝酰(NOCl,沸点为-5.5℃)是有机合成中的重要试剂,为黄色气体,具有刺鼻恶臭味,遇水反应,有多种方法制备氯化亚硝酰。已知:HNO2既有氧化性又有还原性,AgNO2微溶于水,溶于硝酸:AgNO2+HNO3=AgNO3+HNO2。
(1)将5g在300℃下干燥了3h并研细的KCl粉末装入50mL带有接头及抽真空用活塞的玻璃容器内。将容器尽量减压,在减压条件下通入0.002molNO2。反应12~36min即可完成,红棕色的NO2消失,出现黄色的氯化亚硝酰,同时还得到一种盐,该盐的化学式为_。氯化钾需要“干燥”的原因是__。
(2)实验室可由氯气与一氧化氮在常温常压下合成氯化亚硝酰,装置如图所示。

①仪器a的名称为__。
②干燥管中盛放的试剂为_。
③生成NOCl的化学方程式为__。
(3)为验证NOCl与H2O反应后的溶液中存在Cl-和HNO2,设计如下实验步骤,完成下列表格。
步骤 | 实验现象或反应的化学方程式 |
①取5mL仪器a中产品,加入盛有水的烧杯中,充分反应 | NOCl与H2O反应的化学方程式为__ |
②向烧杯中滴加足量AgNO3溶液,有白色沉淀生成,再加入足量稀硝酸 | 加入稀硝酸后,实验现象为__ |
③向步骤②烧杯中滴加酸性KMnO4溶液 | 实验现象为_ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com