
����Ŀ��ҩ��W�Ըΰ������ƾ��кܺõ�Ч����һ�ֺϳ�ҩ��W��·�����£�
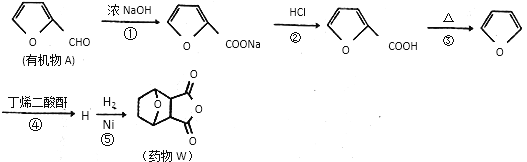
��֪������Ϣ��
��2HCHO+NaOH��CH3OH+HCOONa
��![]()
�۶�ϩ�������ĽṹͲʽΪ![]()
�ش��������⣺
��1���л���A�к��еĹ�������̼̼˫����________(������)��
��2���ڢٲ���Ӧ�г�����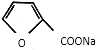 �⣬��������һ����˲���Ľṹ��ʽΪ________��
�⣬��������һ����˲���Ľṹ��ʽΪ________��
��3��H�Ľṹ��ʽΪ___________��
��4���ڢݲ��ķ�Ӧ������____________��
��5��L��ҩ��W��ͬ���칹�壬ͬʱ��������������L��_____��(�����������칹)��
�ٷ����к��б�������������4��ȡ����
�ڼ�����FeCl3��Һ������ɫ��Ӧ��������NaHCO3��Һ��Ӧ��������
��1mol L����3molNaOH��ȫ��Ӧ
���к˴Ź�������Ϊ����壬�������Ϊ1:2:2:3�Ľṹ��ʽΪ_________��
��6��д����![]() �Ʊ���ϩ������
�Ʊ���ϩ������![]() �ĺϳ�·��:___________(�����Լ���ѡ)��
�ĺϳ�·��:___________(�����Լ���ѡ)��
���𰸡� ȩ�����Ѽ� ![]()
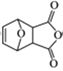 �ӳɷ�Ӧ����ԭ��Ӧ�� 16
�ӳɷ�Ӧ����ԭ��Ӧ�� 16 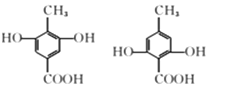
![]()
����������1����ͼʾA�Ľṹ�õ��л���A����̼̼˫����ȩ�����Ѽ����ֹ����š�
��2���ڢٲ���Ӧʵ��Ӧ�ý�����Ŀ����֪��Ϣ�ٵķ�Ӧ��ȩ���������Ʒ�Ӧ�õ������������Σ����������������Ϊ��![]() ��
��
��3��![]() ��
��![]() Ӧ�÷�����Ŀ����֪��Ϣ�ڵķ�Ӧ������
Ӧ�÷�����Ŀ����֪��Ϣ�ڵķ�Ӧ������![]() �е�����˫����
�е�����˫����![]() �е�̼̼˫���ӳɣ��õ���Ԫ�����������HΪ
�е�̼̼˫���ӳɣ��õ���Ԫ�����������HΪ �����巴Ӧ���Բο�����ͼ�Σ�
�����巴Ӧ���Բο�����ͼ�Σ�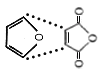 ��
��
��4���ڢݲ��ķ�Ӧ��H��H2��Ӧ���л����������ķ�Ӧֻ�����Ǽӳɷ�Ӧ��
��5��W�ķ���ʽΪC8H8O4����5�������Ͷȡ�������Ŀ�������������õ�L��һ���б�����4�������Ͷȣ����з��ǻ������Ȼ���1�������Ͷȣ��������ΪҪ��Ӧ3mol�������ƣ�����ֻ���DZ���������2�����ǻ���һ���Ȼ���һ���������������������ǻ���һ���Ȼ��Ľṹ��6�֣���ÿ�ֽṹ�����ۼ���λ�ã��õ����½�������Ǵ������Ŀ���λ�ã���
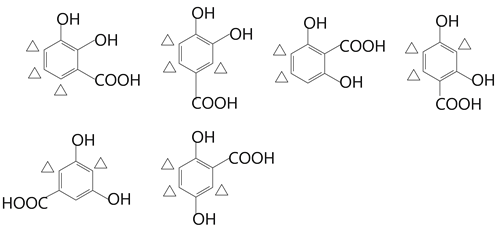
���Դ�Ϊ16�֡����к˴Ź�������Ϊ����壬�������Ϊ1:2:2:3�ģ�Ӧ�������жԳ��ԱȽϺõĽṹ��������ṹ��ʽΪ�� ��
��
��6��������Ŀ�ķ�Ӧ�۽�![]() ֱ�Ӽ��ȿ�����ȥ�Ȼ����ٽ���1,4-�ӳɣ�ˮ�⣬�������ɡ�����·��ͼΪ��
ֱ�Ӽ��ȿ�����ȥ�Ȼ����ٽ���1,4-�ӳɣ�ˮ�⣬�������ɡ�����·��ͼΪ��![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(һ)ij��ѧ��ȤС�������ͼʾʵ��װ��(ͼ��ʡ���˼г�����)���ⶨij��̼�Ͻ�����������������
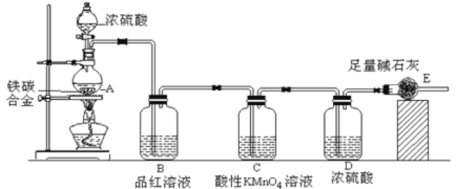
(1)����A��������___________��
(2)Cװ�õ�����______________��
(3)��С��ͬѧ��Ƶ�ʵ��װ�ô���ȱ�ݣ��йظ�ʵ��װ�ü�ʵ������У��������ؿ��ܻᵼ����������������ֵƫ�͵���___________��
A��A�з�Ӧ����ȫ
B����Ӧ���ɵ�SO2���ֱ�E�м�ʯ������
C��E�м�ʯ�һ����տ����е�CO2��H2O
D����Ӧ��ȫ����CO2����������װ����ϵ��
(��)��19.20 g CuO��Fe2O3�Ļ�����ڸ�������������CO��ַ�Ӧ����Ӧ��ȫ��������200 mL 1.20 molL-1 Ba(OH)2��Һ���գ�����35.46 g��ɫ����(�����dz������ܽ⣬������Һ����ı仯)��
(4)�������������Һ�����ʵĻ�ѧʽΪ________����Ũ��Ϊ_________��
(5)�������CuO��Fe2O3�����ʵ���֮��Ϊ__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͭ������ˮ����130��ʱ�ᷢ���ֽⷴӦ����һ��ȼ�մ�������ʳ�ε�Ϊԭ���Ʊ�������ͭ[Cu(ClO4)2��6H2O]��һ�ֹ�����������:

(1)���������I��ʱ�����õĽ���Ĥ��_______________(������ӽ���Ĥ���������ӽ���Ĥ��)��
(2)�绯��Ӧ��ͬһ��������ͬ��Ԫ��������������ԭ��Ӧ����֪�������������С��绯��Ӧ���IJ���֮һΪNaClO3��
�١��绯��Ӧ���Ļ�ѧ����ʽΪ____________________________��
�ڡ��绯��Ӧ���������õIJ�ͬ�¶ȶԲ���Ӱ��Ľ����ͼ��ʾ����÷�Ӧ�����˵��¶���___��

(3)�����II������������Ϊ______________(�����ӷ���)��
(4)����a�IJ���������_______���������п�ѭ�����õ�������_____________(�ѧʽ)��
(5)�øù��������Ʊ�������ͭʱ������ʼʱNaCl������Ϊat�������Ƶõ�Cu(ClO4)2��6H2OΪbt�������Ϊ__________(�ú�a��b�Ĵ���ʽ��ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ȡ�봢��������Դ����������о��ȵ㡣�ش���������:
��1��ֱ���ȷֽⷨ����
ij�¶�����2H2O(g)![]() 2H2(g)+O2(g)���÷�Ӧ��ƽ�ⳣ������ʽΪK=______��
2H2(g)+O2(g)���÷�Ӧ��ƽ�ⳣ������ʽΪK=______��
��2���Ҵ�ˮ������������
��Ӧ���̺ͷ�Ӧ��ƽ�ⳣ��(K)���¶�(T)�ı仯������ͼ1��ʾ��ij�¶�����ͼ1��ʾ��Ӧÿ����1molH2(g)�������仯��62kJ����÷�Ӧ���Ȼ�ѧ����ʽΪ_____________��
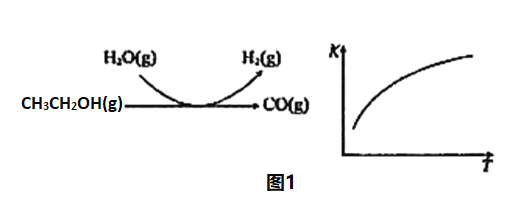
��3��ˮú��������
CO(g)+H2O(g)![]() CO2(g)+H2(g) ��H<0
CO2(g)+H2(g) ��H<0
�ڽ�����[n(CO):n(H2O)]��ͬʱ�������Ӧ��CO��ƽ��ת���ʼ�ͼ2(ͼ�и����Ӧ�ķ�Ӧ�¶ȿ�����ͬ��Ҳ���ܲ�ͬ)��
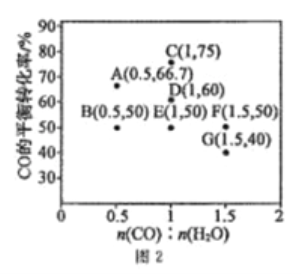
����2L���º����ܱ������м���һ������CO��0.1molH2O(g)����ͼ��G���Ӧ�¶�������Ӧ��5min�ﵽƽ������ƽ����Ӧ����v(CO)=________��
��ͼ��B��E�����Ӧ�ķ�Ӧ�¶ȷֱ�ΪTB��TE����TB_____TE(����>����<������=��)��
�۾�������A��E��G�����Ӧ�ķ�Ӧ�¶ȶ���ͬ(��ΪT��)����ԭ����A��E��G�����Ӧ��_________��ͬ��
�ܵ�T��ʱ������һ�ݻ��ɱ���ܱ�������ͬʱ����3.0molCO��1.0molH2O(g)��1.0molCO2��x molH2��Ϊʹ������Ӧ��ʼʱ������Ӧ�����������xӦ�����������______��
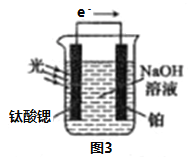
��4����绯ѧ�ֽ�����
��Ӧԭ����ͼ3�������ȹ�缫�ĵ缫��ӦʽΪ4OH-��4e����O2����2H2O���缫�ĵ缫��ӦʽΪ________________��
��5��Mg2Cu��һ�ִ���Ͻ�350��ʱ��Mg2Cu��H2��Ӧ������MgCu2�ͽ���һ�ֽ���Ԫ�ص��⻯��(���������������ԼΪ7.7%)���÷�Ӧ�Ļ�ѧ����ʽΪ______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±��dz����£�Ũ��Ϊ0.01mol/L��NaOH��Һ�뼸������λ�Ϻ�����:
������ | ���ǰ����ε���Ũ�� | ��ϱ����������Һ���� |
�� | c(HA)=0.02mol/L | �������ϣ�pH>7 |
�� | HB��Һ��pH=2 | V1mLNaOH��Һ��V2mLHB��Һ��pH=7 |
�� | c(H2C)=0.01mol/L | �������ϣ�pH>7 |
�� | c(NaHD)=0.01mol/L | �������ϣ�pH=7 |
�ش���������:
(1)������Һ�У�HA��A-��Na+��������Ũ���ɴ�С��˳��Ϊ________����pH=8����c(Na+)-c(A-)=________mol/L(���������)��
(2)�ɢ�����ҺpH=7����֪��V1____V2��
(3)������Һ�У�pH>7��ԭ����______________________��
(4)0.01mol/LNaHD��Һ�У�ˮ�ĵ����=_________��(��֪:ˮ�ĵ����=[�ѵ����ˮ���ӵĸ���/ˮ��������]��100%)
(5)��ƾ���������һ����ȷ��HA��HB��H2C��H2D�������������������_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ�ڸ�ϰԪ�ػ����������ʱ����������ѧϰ�ʼǣ�����һ����ɡ�
��1����������ɫΪ__________�����ȵ�ԭ�ӽṹʾ��ͼ�Ʋ⣬�������к�ǿ��______ �ԡ�Ϊ��֤���Ʋ��Ƿ���ȷ����������ʵ�飺
I�������ȵ���˿����ʢ�������ļ���ƿ���۲���˿��������ȼ�գ��д����ػ�ɫ�̡��÷�Ӧ�Ļ�ѧ����ʽ��___________��
II���ڿ����е�ȼH2��Ȼ���ܻ�������ʢ�������ļ���ƿ���ɹ۲쵽H2�������а���ȼ�գ�����______ɫ�Ļ��棬ƿ���а���������
��ʵ��I��II��֪�������Ʋ�_____�����ȷ������ȷ������������_____��
III������������ˮ���Ƶ���ˮ���������ʲ�����������ˮ��Ӧ����_____��
Na2CO3��Һ B��FeCl2��Һ C��AgNO3 ��Һ D��CuCl2��Һ
��2��������һЩ��������֮���ת����ϵ��A��һ�ֺ�ɫ������FΪ��������İ�ɫ������B��C������ǿ�ᡣ��ͼ�в��ֲ��P��Ӧ������ȥ��
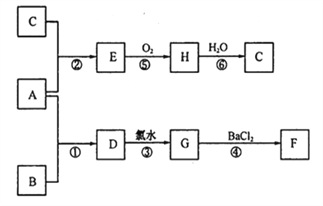
��A��B �ֱ�Ϊ��A_________ B_________��
��A��B������Ӧ��������__________________��
�۷�Ӧ�Ļ�ѧ����ʽΪ_____________________��
��������Ӧ�У�������������ԭ��Ӧ����_______________������������ţ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��W��X��Y��Z�Ƕ�����Ԫ�أ�W��һ��ͬλ�������ӣ�X�ĵ����ڿ����к���Լռ78%��Y�ĵ����ڿ�����ȼ�շ���ҫ�۰⣬Z�ĵ������ڹ�ҵ��Ư�ۡ�����˵���������
A. W��X�γɵĻ������п��ܼȴ��ڼ��Լ����ִ��ڷǼ��Լ�
B. �����������Zһ������X
C. ��ҵ�ϲ�ȡ�������Y��Z������ķ���ұ��Y
D. W��X�Ļ�������W��Z�Ļ����ﷴӦ�ɲ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij������Է�������Ϊ86�������к���1��-CH2-��4��-CH3�������һ�ȴ���Ľṹ��(�����������칹)�� ��
A.2��
B.3��
C.4��
D.5��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ˮ��ɽ���ǽ�ɽ��ɽ����������,��ɫ��չ����̬������Ϊ�й�չʾ�������һ���¡���Ƭ��������β������ɴ�����Ⱦ����Ҫԭ��֮һ,���ٵ����������ڴ����е��ŷ��ǻ�����������Ҫ����֮һ����ش��������⣺
(1)��֪��N2(g)+O2(g)=2NO(g)��H1=+180.5kJ/mol
C(s)+O2(g)=CO2(g)��H2=-393.5kJ/mol
2C(s)+O2(g)=2CO(g)��H3=-221kJ/mol
��ij��Ӧ��ƽ�ⳣ������ʽΪ��K=[c(N2) ��c2(CO2)]/[c2(NO) ��c2(CO)],��˷�Ӧ���Ȼ�ѧ����ʽΪ____________________________________��
(2)N2O5��һ�������¿ɷ����ֽ⣺2N2O5(g)![]() 4NO2(g)+O2(g),ij�¶��º����ܱ������м���һ����N2O5,���N2O5Ũ����ʱ��ı仯���±���
4NO2(g)+O2(g),ij�¶��º����ܱ������м���һ����N2O5,���N2O5Ũ����ʱ��ı仯���±���
t/min | 0 | 1 | 2 | 3 | 4 | 5 |
c(N2O5)/<mol��L-1) | 1.00 | 0.71 | 0.50 | 0.35 | 0.25 | 0.17 |
�ٷ�Ӧ��ʼʱ��ϵѹǿΪp0,��2minʱ��ϵѹǿΪp1����p1��p0=__________��2~5min����NO2��ʾ�ĸ÷�Ӧ��ƽ����Ӧ����Ϊ__________��
��һ���¶��£��ں����ܱ������г���һ����N2O5���и÷�Ӧ,���жϷ�Ӧ�Ѵﵽ��ѧƽ��״̬����__________��(����ĸ)��
a��NO2��O2��Ũ�ȱȱ��ֲ��� b��������ѹǿ���ٱ仯
c��2v��(NO2)=v��(N2O5) d��������ܶȱ��ֲ���
(3)Kp���÷�Ӧ��ϵ���������ʵķ�ѹ����ʾ��ƽ�ⳣ��������K����ʽ��ƽ��Ũ����ƽ���ѹ���档��֪��Ӧ��NO2(g)+CO(g)![]() NO(g)+CO2(g),�÷�Ӧ������Ӧ����v��=k����p(NO2)��p(CO),�淴Ӧ����v��=k����p(NO)��p(CO2),����k����k��Ϊ���ʳ���,��KpΪ__________(��k����k����ʾ)��
NO(g)+CO2(g),�÷�Ӧ������Ӧ����v��=k����p(NO2)��p(CO),�淴Ӧ����v��=k����p(NO)��p(CO2),����k����k��Ϊ���ʳ���,��KpΪ__________(��k����k����ʾ)��
(4)��ͼ���ܱշ�Ӧ���а�n(N2) ��n(H2)=1��3Ͷ�Ϻ�,��200�桢400�桢600����,�ϳ�NH3��Ӧ�ﵽƽ��ʱ,�������NH3�����ʵ���������ѹǿ�ı仯���ߣ���֪�÷�ӦΪ���ȷ�Ӧ��
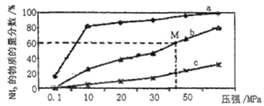
������a��Ӧ���¶���__________��
��M���Ӧ��H2��ת������__________��
(5)��ҵ�ϳ��ð�ˮ���ն�������,������(NH4)2SO3���жϳ�����(NH4)2SO3��Һ������Բ�˵���ж����ݣ�______________________________________________��(��֪��NH3��H2O��Kb=1.8��10-5;H2SO3��Ka1=1.3��10-2,Ka2=6.3��10-8��)
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com