
| 1+3+16 |
| a+b+c |
| V |
| 1.1V |


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| ģ�⺣ˮ�е�����Ũ�ȣ�mol/L�� | Na+ | Mg2+ | Ca2+ | Cl- | HCO3- |
| 0.439 | 0.050 | 0.011 | 0.560 | 0.001 |
| A��������XΪCaCO3 |
| B����ҺM�д���Mg2+��Ca2+ |
| C����ҺN�д���Mg2+��Ca2+ |
| D�������������Ϊ����4.2g NaOH���壬������Yֻ��Mg��OH��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 �״�-����ȼ�ϵ�أ�DMFC����һ�ָ�Ч�ܡ�����Ⱦ�ij��ص�أ��õ���������ӽ���Ĥ����H+������ܷ�ӦΪ��2CH3OH+3O2=2CO2��g��+4H2Oij��ѧ��ȤС��ͬѧ�о��״�-����ȼ�ϵ��ԭ��������һ�����е绯ѧʵ�飬��ʵ��װ��ʾ��ͼ��ͼ��
�״�-����ȼ�ϵ�أ�DMFC����һ�ָ�Ч�ܡ�����Ⱦ�ij��ص�أ��õ���������ӽ���Ĥ����H+������ܷ�ӦΪ��2CH3OH+3O2=2CO2��g��+4H2Oij��ѧ��ȤС��ͬѧ�о��״�-����ȼ�ϵ��ԭ��������һ�����е绯ѧʵ�飬��ʵ��װ��ʾ��ͼ��ͼ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ������ | Ag+ Na+ |
| ������ | NO3- SO42- Cl- |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��-770 kJ/mol |
| B��-l220 kJ/mol |
| C��-1500kJ/mol |
| D��-2740kJ/mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������ˮ�е��뼸�α���FeCl3��Һ�������������Һ�ʺ��ɫ�����Ƶ�Fe��OH��3���� |
| B��CO2����ˮ�У�ֻ���ڣ�CO2+H2O?H2CO3ƽ�� |
| C���ڳ�ʪ�Ŀ����У������ȴ�������ʴ |
| D��ʵ���ҿ���ŨH2SO4�Ʊ�HCl��������ΪH2SO4�����Ա�HClǿ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
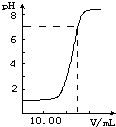 ��ͼ����25.00mL����������NaOH��Һʱ����ҺpH�仯��ͼ����ͼ����������н����в���ȷ���ǣ�������
��ͼ����25.00mL����������NaOH��Һʱ����ҺpH�仯��ͼ����ͼ����������н����в���ȷ���ǣ�������| A��������ʼŨ��Ϊ0.10 mol?L-1 |
| B��NaOH��ҺŨ��Ϊ0.10 mol?L-1 |
| C���ε��е�ʱ����NaOH���ʵ���Ϊ0.0025mol |
| D���������Ϊ20.00mLʱ��������Һ�е���2�η�̪��Һ����Һ�Ժ�ɫ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com