
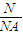 =
=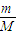 =
=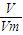 =CV.
=CV.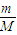 求得24g镁的物质的量为1mol,Mg原子失去2个电子成Mg2+,故24g镁失去的电子数为2NA,故A错误;
求得24g镁的物质的量为1mol,Mg原子失去2个电子成Mg2+,故24g镁失去的电子数为2NA,故A错误;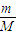 求得18g水的物质的量为1mol,故18g水所含的电子数目为10NA,故B错误;
求得18g水的物质的量为1mol,故18g水所含的电子数目为10NA,故B错误;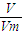 中气体摩尔体积Vm在标准状况下为22.4L/mol,常温常压下气体摩尔体积Vm不知道,因此无法求出常温常压下11.2L二氧化碳气体物质的量,所含的分子数目也无法求出.故C错误;
中气体摩尔体积Vm在标准状况下为22.4L/mol,常温常压下气体摩尔体积Vm不知道,因此无法求出常温常压下11.2L二氧化碳气体物质的量,所含的分子数目也无法求出.故C错误;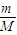 求得32g氧气物质的量为1mol,而O2中含有2个O原子,则32g氧气所含的原子物质的量为2mol,所含原子数目为2NA,故D正确.
求得32g氧气物质的量为1mol,而O2中含有2个O原子,则32g氧气所含的原子物质的量为2mol,所含原子数目为2NA,故D正确.

 名校课堂系列答案
名校课堂系列答案湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com