
| A、两种微粒,若核外电子排布完全相同,则其化学性质相同 |
| B、凡单原子形成的稳定离子,一定具有稀有气体元素原子的核外电子排布 |
| C、K+与Cl-通过静电引力结合形成离子化合物KCl |
| D、离子化合物中可以含有共价键,但共价化合物中一定不含离子键 |


科目:高中化学 来源: 题型:
| A、+1 | B、+5 | C、+3 | D、+4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、放电时,正极发生氧化反应 |
| B、放电时,把热能转化为电能 |
| C、充电时,电池的负极发生还原反应 |
| D、充电时,把化学能转化为电能 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、锌锰干电池工作一段时间后碳棒变细 |
| B、氢氧燃料电池工作时氢气在负极被氧化 |
| C、太阳能电池的主要材料是高纯度的二氧化硅 |
| D、氢氧燃料电池可将热能直接转变为电能 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、检验乙醛中的醛基:在一定量CuSO4溶液中,加入少量NaOH溶液,然后再加入乙醛,加热产生砖红色沉淀 |
| B、分离提纯苯:向苯和苯酚混合溶液中加入足量浓溴水,静置后分液 |
| C、比较CH3COO-和CO32-结合H+的能力:相同温度下,测定浓度均为0.1mol?L-1的Na2CO3和CH3COONa溶液的pH |
| D、检验溴乙烷中的溴元素:向某溴乙烷中加入NaOH溶液共热,冷却后滴入AgNO3溶液,观察有无浅黄色沉淀生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | +2 | -2 |
| A、R的氧化物对应的水化物可能具有两性 |
| B、L、Q形成的简单离子核外电子数相等 |
| C、T、Q的氢化物常态下均为无色气体 |
| D、L、M的单质与稀硫酸反应速率:M>L |
查看答案和解析>>
科目:高中化学 来源: 题型:
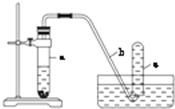 用如图所示的装置进行实验:
用如图所示的装置进行实验:查看答案和解析>>
科目:高中化学 来源: 题型:
| 阳离子 | K+,Ba2+Fe2+Al3+ Fe3+ Mg2+ | ||||
| 阴离子 | OH-HCO
|
- 3 |
2- 3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com