
����Ŀ����֪������(H3PO3)�Ľṹ��ͼ![]() ������ǿ��ԭ�Ե����ᣬ���Ա�����������Ϊ���ᡣ
������ǿ��ԭ�Ե����ᣬ���Ա�����������Ϊ���ᡣ
��1����֪���������PCl3ˮ����ɣ���д����Ӧ�����ӷ���ʽ____________��
��2��Na2HPO3��________(����Ρ�����ʽ�Ρ�)��
��3���������������ӷ�Ӧʱ�������뻹ԭ�������ʵ���֮��Ϊ______________��
��4��ij�¶��£�0.10molL-1��H3PO3��Һ��pHΪ1.6����c(H+)=2.5��10-2molL-1�����¶���H3PO3��һ������ƽ�ⳣ��Ka1=___________________��(H3PO3�ڶ���������Բ��ƣ����������λ��Ч����)
��5����H3PO3��Һ�еμ�NaOH��Һ�����ԣ�������Һ�У�c(Na+)_____c(H2PO3-)+2c(HPO32-)(���������������=��)��
��6����ijŨ�ȵ��������еμ�NaOH��Һ����pH����Һ�е�H3PO3��H2PO3-��HPO32-�����ʵ�������a(X)��ƽ��ʱij���ֵ�Ũ������������Ũ��֮�͵ı�ֵ)�Ĺ�ϵ��ͼ��ʾ��
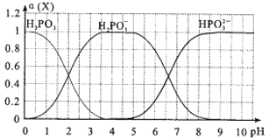
�Է�̪Ϊָʾ��������Һ����ɫ��Ϊdz��ɫʱ��������Ҫ��Ӧ�����ӷ���ʽ��_________________________��
���𰸡�PCl3+3H2O��H3PO3+3H++3Cl- ���� 2��1 8.3��10-3 mol��L-1 = H2PO3-+OH-��HPO32-+H2O
��������
(1)PCl3ˮ�����ȡ����������
(2)����������(H3PO3)�Ľṹ![]() ���ṹ�к���2���ǻ����Ƕ�Ԫ���
���ṹ�к���2���ǻ����Ƕ�Ԫ���
(3)������(H3PO3)����ǿ��ԭ�Ե����ᣬ���Ա�����������Ϊ���ᣬAg+����ԭ����Ag������ת�Ƶ����غ�����������뻹ԭ�������ʵ���֮�ȣ�
(4)��������Һ����̶Ƚ�С�����Ը���Һ�д���c(H2PO3-)��c(H+)=2.5��10-2molL-1��c(H3PO3)=(0.10-2.5��10-2)mol/L����ϵ���ƽ�ⳣ������ʽ���㣻
(5)��H3PO3��Һ�еμ�NaOH��Һ�����ԣ���c(H+)=c(OH-)����ϵ���غ��жϣ�
(6)��̪�ı�ɫ��ΧΪ8-10���Է�̪Ϊָʾ��������Һ����ɫ��Ϊdz��ɫʱ����Һ��pH����8������ͼ����Һ��H2PO3-ת��ΪHPO32-���ݴ���д��Ӧ�ķ���ʽ��
(1)PCl3ˮ�����ȡ����������ᣬ��Ӧ�����ӷ���ʽΪPCl3+3H2O��H3PO3+3H++3Cl-���ʴ�Ϊ��PCl3+3H2O��H3PO3+3H++3Cl-��
(2)����������(H3PO3)�Ľṹ![]() ���ṹ�к���2���ǻ����Ƕ�Ԫ���ᣬ��ö�Ԫ��������������������ӣ�Na2HPO3�Ǹö�Ԫ�����е�Hԭ�Ӳ��ܱ����룬����Na2HPO3Ϊ���Σ��ʴ�Ϊ�����Σ�
���ṹ�к���2���ǻ����Ƕ�Ԫ���ᣬ��ö�Ԫ��������������������ӣ�Na2HPO3�Ǹö�Ԫ�����е�Hԭ�Ӳ��ܱ����룬����Na2HPO3Ϊ���Σ��ʴ�Ϊ�����Σ�
(3)�������������ӷ�Ӧ�������ᣬ�����ӻ�ԭΪ�����ʣ���Ӧ��������������������H3PO3�ǻ�ԭ��������ת�Ƶ����غ㣬n(Ag+)=n(H3PO3)��(5-3)�����n(Ag+)��n(H3PO2)=2��1���ʴ�Ϊ��2��1��
(4)��������Һ����̶Ƚ�С�����Ը���Һ�д���c(H2PO3-)��c(H+)=2.5��10-2molL-1��c(H3PO3)=(0.10-2.5��10-2)mol/L�������ƽ�ⳣ��K=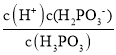 =
=![]() =8.3��10-3 mol/L���ʴ�Ϊ��8.3��10-3 mol/L��
=8.3��10-3 mol/L���ʴ�Ϊ��8.3��10-3 mol/L��
(5)��H3PO3��Һ�еμ�NaOH��Һ�����ԣ���c(H+)=c(OH-)����Һ�д��ڵ���غ㣬���ݵ���غ���c(Na+)=c(H2PO3-)+2c(HPO32-)���ʴ�Ϊ��=��
(6)��̪�ı�ɫ��ΧΪ8-10���Է�̪Ϊָʾ��������Һ����ɫ��Ϊdz��ɫʱ����Һ��pH����8������ͼ����Һ��H2PO3-ת��ΪHPO32-���������ӷ���ʽΪH2PO3-+OH-��HPO32-+H2O���ʴ�Ϊ��H2PO3-+OH-��HPO32-+H2O��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��H2SΪ��Ԫ���ᡣ20 ��ʱ����0.100 mol��L��1��Na2S��Һ�л���ͨ��HCl����(������Һ����ı仯��H2S�Ļӷ�)������ָ����Һ���������ʵ���Ũ�ȹ�ϵһ����ȷ����(����)
A. ͨ��HCl����֮ǰ�� c(S2��)>c(HS��)>c(OH��)>c(H��)
B. c(HS��)��c(S2��)�ļ�����Һ�У� c(Cl��)��c(HS��)>0.100 mol��L��1��c(H2S)
C. pH��7����Һ�У� c(Cl��)��c(HS��)��2c(H2S)
D. c(Cl��)��0.100 mol��L��1����Һ�У� c(OH��)��c(H��)��c(H2S)��c(S2��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������[CO(NH2)2]���ǵ�����Ҫ������ڹ�ũҵ������Ӧ�ù㷺��
(1)��֪��N2(g)��3H2(g)![]() 2NH3(g)��H����92kJ��mol-1
2NH3(g)��H����92kJ��mol-1
��ȡ1molN2(g)��3molH2(g)����һ�ܱ������У��ڴ�������ʱ���з�Ӧ����÷�Ӧ�ų�������___92.2kJ(������������������������)��ԭ����_______________��
��ʹ�ô������÷�Ӧ��H_____(�������������С������������)��
����֪���ֱ��ƻ�1molN��N����1molH��H����Ҫ���յ�����Ϊ��946kJ��436kJ�����ƻ�1molN��H����Ҫ���յ�����Ϊ_____kJ��
(2)��CO2��NH3Ϊԭ�Ͽɺϳɻ�������[CO(NH2)2]����֪��
��.2NH3(g)+CO2(g)==NH2CO2NH4(s)��H����159.5kJ/mol
��.NH2CO2NH4(s)==CO(NH2)2(s)+H2O(g)��H��+116.5kJ/mol
��.H2O(l)==H2O(g)��H��+44.0kJ/mol
��д��CO2��NH3�ϳ����غ�Һ̬ˮ���Ȼ�ѧ��Ӧ����ʽ_______________________��
�ڻ�ѧ�������о����ض���ȼ�ϵ�ء������ֵ��ֱ��ȥ�����з�ˮ�е����أ����ܲ���������ˮ�����ܷ��磬����ȼ�ϵ�ؽṹ��ͼ��ʾ��
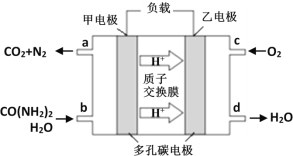
�ش��������⣺
����еĸ���Ϊ_____(����������������)���ĵ缫��ӦʽΪ_____________��
��ع���ʱ��������ÿ����1mol���أ�����O2�����(��״����)ԼΪ_____L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ƽ����ϵCa(OH)2(s)![]() Ca2+ +2OHһ�У���ʹc(Ca2+)��С����ʹc(OHһ)�������
Ca2+ +2OHһ�У���ʹc(Ca2+)��С����ʹc(OHһ)�������
A. ��������MgCl2���� B. ��������Na2CO3����
C. ��������KCl���� D. ��������ϡH2SO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼ��ʾװ�ûش��������⡣��֪����KMnO4��������Ũ���ᷴӦ���Ƶ�Cl2����H2SiO3������ˮ��
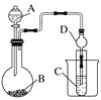
(1)������ͼװ�ÿ�����֤Ԫ�طǽ����Եı仯���ɡ�ͼ��Aװ�õ�������________________�������D��������____________��
(2)ʵ����������ҩƷNa2S��KMnO4��Ũ���ᡢMnO2����ѡ�����ҩƷ���ʵ����֤�ȵķǽ�����ǿ������ƿ�з�����Ӧ�����ӷ���ʽΪ____________________________��װ��C�е�ʵ������Ϊ�е���ɫ�������ɣ����ӷ���ʽΪ_____________________��
(3)��Ҫ�ô�װ��֤�����ԣ�HNO3��H2CO3��H2SiO3������֤���ǽ����ԣ�N��C��Si������������������ѡ����ͬѧ��Ƶ�ʵ�����õ������ʣ���ϡHNO3����ϡ���ᡡ��̼��ơ���Na2SiO3��Һ����SiO2���Լ�A��C�ֱ�Ϊ________(�����)���Թ��з�����Ӧ�����ӷ���ʽΪ__________________����ͬѧ��Ϊ��ʵ�鲻��˵��N��C��Si�ķǽ�����ǿ��������Ϊԭ����_____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������о�������������ˮ��SO2���γɵ���Һ�д���������ƽ�⣺

�ݴˣ������ж�����ȷ����( )
A������Һ�д�����SO2����
B������Һ��H��Ũ����SO32��Ũ�ȵ�2��
C�������Һ�м����������ᶼ�ܷų�SO2����
D�������Һ�м������NaOH�ɵõ�Na2SO3��NaHSO3��NaOH�Ļ����Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������20.00 mL 0.1000 mol��L��1 (NH4)2SO4��Һ����μ���0.2000 mol��L��1NaOHʱ����Һ��pH������NaOH��Һ����Ĺ�ϵ����ͼ��ʾ�������ǻӷ���������˵����ȷ����

A����a��ʾ��Һ�У�c(NH4+)��c(SO42-)��c(H+)��c(OH��)
B����b��ʾ��Һ�У�c(NH4+)��c(Na��)��c(H��)��c(OH��)
C����c��ʾ��Һ�У�c(SO42-)+ c(H+)�� c(NH3��H2O )+ c(OH��)
D����d��ʾ��Һ�У�c(SO42-)��c(NH3��H2O )��c(OH��)��c(NH4+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��W��X��Y��Z��ԭ�������������ӡ�m��p��r������ЩԪ����ɵĶ�Ԫ�����n��Ԫ��Z�ĵ��ʣ�ͨ��Ϊ����ɫ���壬q��ˮ��Һ����Ư���ԣ�0.01mol��L-1r��Һ��pHΪ2��sͨ����������ˮ�Ļ����������ʵ�ת����ϵ��ͼ��ʾ������˵����ȷ���ǣ� ��

A. ԭ�Ӱ뾶�Ĵ�СW <X<Y B. Ԫ�صķǽ�����Z>X>Y
C. Y���⻯�ﳣ�³�ѹ��ΪҺ̬ D. X������������ˮ����Ϊǿ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ƶ�˼ά�����ڻ�ѧѧϰ���о�����ʱ���������Ľ��ۣ��������Ƴ��Ľ�������Ҫ����ʵ���ļ�����ܾ�������ȷ����������ƽ�������ȷ���ǣ� ��
A��Mgʧ������CO2���Naʧ��Ҳ������CO2���
B��Fe3O4��д��FeO��Fe2O3��Pb3O4Ҳ��д��PbO��Pb2O3
C��Cu��Cl2ֱ�ӻ�������CuCl2��Cu��Sֱ�ӻ���Ҳ�ܵõ�CuS
D��CO2ͨ�뵽���ᱵ��Һ�в������ɳ�����SO2ͨ�뵽���ᱵ��Һ��Ҳ�������ɳ���
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com