

| A�� | ��������KMnO4��Һ���������Ӧ�Ƿ��а�κ������ | |
| B�� | �����ء���κ�������Na2CO3��NaOH��Һ��Ӧ | |
| C�� | ͨ�������£������ء���κ�ᶼ�ܷ���ȡ�����ӳɡ���ȥ��Ӧ | |
| D�� | �������ػ�Ϊͬ���칹�壬��������4�ֲ�ͬ��ѧ�������⣬���ܷ���������Ӧ�ķ�����ﹲ��8�� |
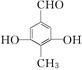
���� A����κ���к���̼̼˫�����������к���ȩ�������ǻ�������ʹ���Ը��������ɫ��
B�������غ��з��ǻ�����κ���еķ��ǻ����Ȼ�������̼���ơ��������Ʒ�Ӧ��
C�����ܷ�����ȥ��Ӧ��
D������������� ��
�� ���֣�
���֣�
��� �⣺A����κ���к���̼̼˫�����������к���ȩ�������ǻ�������ʹ���Ը��������ɫ�����ܼ��𣬹�A����
B���������еķ��ǻ��Ͱ�κ���еķ��ǻ����Ȼ���������̼���ƺ�����������Һ��Ӧ����B��ȷ��
C�������غͰ�κ����Է���ȡ���ͼӳɷ�Ӧ�����ܷ�����ȥ��Ӧ����C����
D���������ػ�Ϊͬ���칹�壬��������4�ֲ�ͬ��ѧ�������⣬���ܷ���������Ӧ��˵���ṹ�Գƣ�����ȩ��������������� ��
�� ���֣���D����
���֣���D����
��ѡB��
���� ���⿼���л���Ľṹ�����ʣ��Ǹ߿��еij������ͺ���Ҫ�Ŀ���֮һ������Ĺؼ���ȷ�жϳ������к��еĹ����ţ�Ȼ��������Ӧ�����ŵĽṹ�����ʣ�������ü��ɣ�����������ѧ����֪ʶǨ�������ͼ�����������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2-�������һ�������4�� | |
| B�� | ��ϩ�;�����ϩ����ʹ��ˮ��ɫ | |
| C�� | �Ҵ�������ȿ���NaOH���֣�Ҳ������С�մ����� | |
| D�� | �����������ܷ����ӳɷ�Ӧ���ܷ���ˮ�ⷴӦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ijЩ����ʯ����뱣�${\;}_{86}^{222}$Rn �����Ӷ�����������˺���${\;}_{86}^{222}$Rn���������� 222 | |
| B�� | Se ������������Ԫ�أ�${\;}_{34}^{78}$Se ��${\;}_{34}^{80}$Se ��Ϊͬλ�� | |
| C�� | ${\;}_{92}^{235}$U ��Ũ��һֱ����������ע��${\;}_{92}^{235}$U �� ${\;}_{92}^{238}$U �����ֲ�ͬ�ĺ��� | |
| D�� | ${\;}_{6}^{13}$C-NMR���˴Ź������ں�̼������Ľṹ������${\;}_{6}^{13}$C ��������Ϊ 6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����װ������KClO3��ȡO2��װ����ͬ | |
| B�� | ����Ũ������ﰱ�� | |
| C�� | ���������ſ������ռ����� | |
| D�� | ����������������պ��Ũ����IJ����������Թܿڸ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 2015�꣬�й���ѧ����������������ű����ҩ�������ػ����ŵ�������������صĽṹ��ͼ��ʾ�������й������ص�˵���в���ȷ���ǣ�������
2015�꣬�й���ѧ����������������ű����ҩ�������ػ����ŵ�������������صĽṹ��ͼ��ʾ�������й������ص�˵���в���ȷ���ǣ�������| A�� | ����ʽΪC15H22O4 | B�� | �����������ܷ���ˮ�ⷴӦ | ||
| C�� | ����������ˮ��ȡֲ���е������� | D�� | �ṹ�к������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ̼�����缫��ⱥ��ʳ��ˮ�������ĵ缫��ӦʽΪ2Cl--2e-�TCl2�� | |
| B�� | ��C��ʯī����s���TC�����ʯ����s����H=+1.90 kJ•mol-1��֪�����ʯ��ʯī�ȶ� | |
| C�� | ��ͭ����ʱ�����������������Ǵ�ͭ���缫��ӦʽΪ��Cu-2e-�TCu2+ | |
| D�� | ��ϡ��Һ�У�H+��aq��+OH-��aq���TH2O��l����H=-57.3KJ/mol����ϡ������ϡNaOH��Һ��Ӧ����1 mol H2O��l��ʱҲ�ų�57.3 kJ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com