
分析 (1)①△H-T△S<0的反应能够自发进行;
②可逆反应达到平衡状态时,正逆反应速率相等(同种物质)或正逆反应速率之比等于系数之比(不同物质),平衡时各种物质的物质的量、浓度等不再发生变化,由此衍生的一些物理量不变,以此分析;
③平衡正向移动可以通过反应物的转化率;
(2)根据热化学方程式的意义以及热化学方程式的书写方法来写;
(3)依据反应方程式计算出反应初始时充入NO2的物质的量浓度,再根据c=$\frac{n}{V}$计算出二氧化氮的初始浓度;根据转化率=$\frac{反应消耗量}{反应初始量}$×100%计算出二氧化氮的转化率;根据K=$\frac{c({N}_{2}{O}_{4})}{c(N{O}_{2})^{2}}$计算出该反应的平衡常数;逆反应的平衡常数和正反应的平衡常数成倒数计算该温度下反应N2O4(g)?2NO2(g)的平衡常数K.
解答 解:(1)△H-T△S<0的反应能够自发进行,该反应△S<0,若反应能够自发进行,△H必须小于0,
故答案为:<;
②A.速率之比等于化学计量数之比,不能说明反应达到平衡状态,故A错误;
B.生成n mol N2O4的同时生成2nmolNO2,说明正逆反应速率相等,反应达到平衡状态,故B正确;
C.密度始终不变,所以密度不变不能说明反应达到平衡状态,故C错误;
D.颜色不变,说明二氧化氮的浓度不变,反应达到平衡状态,故D正确;
E.平均相对分子质量不再改变,说明气体物质的量不变,反应达到平衡状态,故E正确;
答案为:BDE;
③A.减小二氧化氮的浓度,平衡逆向移动,NO2转化率减小,故A错误;
B.降低温度平衡向正向移动,NO2转化率增大,故B正确;
C.增大压强平衡正向移动,NO2转化率增大,故C正确;
D.升高温度,平衡逆向移动,NO2转化率减小,故D错误;
答案为:BC;
(2)1molN2H4(l)与足量N2O4(l)完全反应生成N2(g)和H2O(l),放612.5kJ的热量,其热化学方程式为:2N2H4(l)+N2O4(l)=3N2(g)+4H2O(l)△H=-1225kJ/mol,
故答案为:2N2H4(l)+N2O4(l)=3N2(g)+4H2O(l)△H=-1225kJ/mol;
(3)17℃、1.01×105Pa,往10L密闭容器中充入NO2,达到平衡时n(NO2)=2.0mol,n(N2O4)=1.6mol,根据反应2NO2(g)?N2O4(g)可知反应初始时,充入NO2的物质的量为:2.0mol+1.6mol×2=5.2mol,则充入NO2的物质的量浓度为:$\frac{5.2mol}{10L}$=0.52mol/L;
平衡时消耗二氧化氮的物质的量为1.6mol×2=3.2mol,则NO2的转化率为:$\frac{3.2mol}{5.2mol}$≈61.5%;
该反应的平衡常数为:K=$\frac{c({N}_{2}{O}_{4})}{c(N{O}_{2})^{2}}$=$\frac{\frac{1.6}{10}}{(\frac{2.0}{10})^{2}}$=4;
该温度下反应N2O4(g)?2NO2(g)的平衡常数K′=$\frac{c({N}_{2}{O}_{4})}{c(N{O}_{2})^{2}}$=$\frac{1}{K}$=0.25mol/L,
故答案为:0.52mol/L;61.%;4;0.25.
点评 本题考查较为综合,题目难度中等,涉及化学平衡常数、转化率的计算、热化学方程式书写、反应自发进行的判断、化学平衡及其影响等知识,明确化学平衡常数的概念及表达式为解答关键,注意掌握反应自发进行的判断方法,试题培养了学生的分析、理解能力及灵活应用能力.


 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | NaOH和金属铝 | B. | NaOH 和CO2 | C. | Na2CO3和HCl | D. | Na和O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 操作 | 现象 |
| Ⅰ.向盛有4.0gNa2O2的烧杯中加入50mL蒸馏水 | 剧烈反应,产生的气体能使带火星木条复燃,固体全部溶解后,得到的无色溶液a |
| Ⅱ.向溶液a中滴入两滴酚酞 | 溶液变红,10分钟后溶液颜色明显变浅,稍后,溶液变为无色 |
| Ⅲ.向溶液中加入少量MnO2粉末 | 又有大量气泡产生,产生的气体也能使带火星木条复燃 |
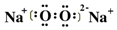 ,很明显,实验证实了溶液a中H2O2的存在,应用同位素示踪原理可以表
,很明显,实验证实了溶液a中H2O2的存在,应用同位素示踪原理可以表查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 78g苯中含有的碳碳双键的数目为3NA | |
| B. | 16g由Cu2S和CuO组成的混合物中含有的阳离子数为0.2NA | |
| C. | 将1molH2与1molI2充入一密闭容器中充分反应后,转移的电子数为2NA | |
| D. | 1mo1Fe与足量的浓硫酸共热反应,生成SO2的分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学键 | H-H | C-O | C≡C | H-O | C-H |
| E/(KJ.mol-1) | 436 | 343 | x | 465 | 413 |
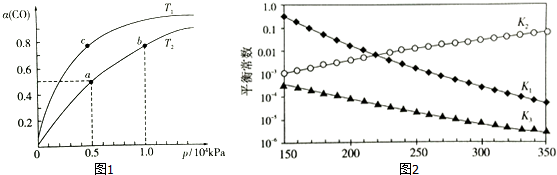
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
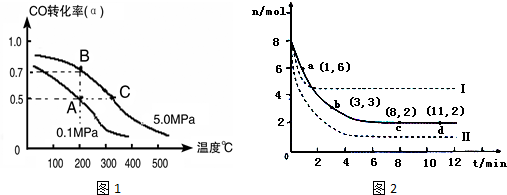
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
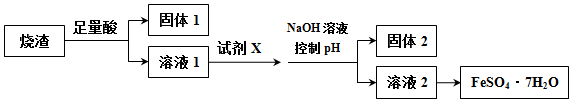
| A. | 溶解烧渣选用足量酸,可以从常见的强酸中选择任意一种,试剂X选用铁粉 | |
| B. | 固体1中一定含有SiO2,控制pH是为了使Al3+转化为Al(OH)3,进入固体2 | |
| C. | 从溶液2得到FeSO4•7H2O产品的过程中,只需要缓慢加热至溶液出现少量晶体,停止加热利用余热蒸干即可 | |
| D. | 若改变方案,在溶液1中直接加NaOH至过量,得到的沉淀用硫酸溶解,其溶液经结晶分离也可得到FeSO4•7H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠与水反应:Na+H2O═Na++OH-+H2↑ | |
| B. | 氢氧化钡溶液与稀硫酸反应:Ba2++SO42-═BaSO4↓ | |
| C. | 碳酸钙与稀盐酸反应:CaCO3+2H+═CO2↑+H2O+Ca2+ | |
| D. | 醋酸与氧化钠反应:Na2O+2H+═2Na++H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com