

 ;
; +2NaOH$→_{△}^{水}$
+2NaOH$→_{△}^{水}$ +2NaBr.
+2NaBr. (写结构简式),其在Fe作催化剂的条件下发生一溴取代,产物只有2种的物质
(写结构简式),其在Fe作催化剂的条件下发生一溴取代,产物只有2种的物质 (写结构简式).
(写结构简式). 分析 有机物X属于芳香化合物,其相对分子质量为120,12gA(即0.1mol)在足量的氧气中充分燃烧后只生成CO220.16L (在标准状况下,即0.9mol)和10.8g (即0.6mol)H2O,根据元素守恒可知,X的化学式为C9H12,有机物X在光照条件下与Cl2反应只能得到2种一氯代物A和B,且这两种一氯代物发生消去反应只能得到一种有机物C.结合题中信息可知,X为 ,A、B为
,A、B为 或
或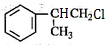 ,C为
,C为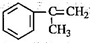 ,根据题中转化关系,C与溴发生加成反应得D为
,根据题中转化关系,C与溴发生加成反应得D为 ,D在碱性溶液中水解得E为
,D在碱性溶液中水解得E为 ,据此答题;
,据此答题;
解答 解:有机物X属于芳香化合物,其相对分子质量为120,12gA(即0.1mol)在足量的氧气中充分燃烧后只生成CO220.16L (在标准状况下,即0.9mol)和10.8g (即0.6mol)H2O,根据元素守恒可知,X的化学式为C9H12,有机物X在光照条件下与Cl2反应只能得到2种一氯代物A和B,且这两种一氯代物发生消去反应只能得到一种有机物C.结合题中信息可知,X为 ,A、B为
,A、B为 或
或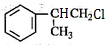 ,C为
,C为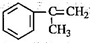 ,根据题中转化关系,C与溴发生加成反应得D为
,根据题中转化关系,C与溴发生加成反应得D为 ,D在碱性溶液中水解得E为
,D在碱性溶液中水解得E为 ,
,
(1)根据上面的分析可知,X的分子式为C9H12,X的结构简式为 ,
,
故答案为:C9H12; ;
;
(2)反应④的化学方程式为 +2NaOH$→_{△}^{水}$
+2NaOH$→_{△}^{水}$ +2NaBr,
+2NaBr,
故答案为: +2NaOH$→_{△}^{水}$
+2NaOH$→_{△}^{水}$ +2NaBr;
+2NaBr;
(3)X属于芳香化合物的同分异构体中,其一氯代物只有2种的物质为 ,其在Fe作催化剂的条件下发生一溴取代,即苯环上的取代,产物只有2种的物质为
,其在Fe作催化剂的条件下发生一溴取代,即苯环上的取代,产物只有2种的物质为 ,
,
故答案为: ;
; ;
;
点评 本题主要考查了学生对有机官能团性质及有机计算的把握情况,具有一定的综合性,只要基础扎实的学生解决这样的问题没什么难度,答题时注意有条件的同分异构体的书写.


科目:高中化学 来源: 题型:多选题
| A. | 沸点低 | B. | 密度比水小 | C. | 乙醇溶于水 | D. | 具有还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②⑦ | B. | ②⑤ | C. | ①③⑤ | D. | ②④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O | B. | HNO3+NaOH═NaNO3+H2O | ||
| C. | CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O | D. | 2FeCl3+Fe═3FeCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题

| A. | OE段化学反应速率最快 | |
| B. | EF段收集CO2气体最多 | |
| C. | 为了加快反应速率,可向溶液中滴入硫酸铜溶液 | |
| D. | 分析OE、EF、FG三段,该反应为放热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a原子电子层数比b原子的电子层数多 | |
| B. | a原子的最外层电子数比b原子的最外层电子数少 | |
| C. | 1mol a 从酸中置换出的H2比1 mol b从酸中置换出的H2多 | |
| D. | 常温时,a能从水中置换出氢气,而b不能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石油裂解的目的是获得更多的轻质液体燃料 | |
| B. | 石油裂化主要是得到乙烯、丙烯等小分子烃 | |
| C. | 石油分馏是物理变化,可分离得到汽油、柴油、煤油等多种馏分,它们都是纯净物 | |
| D. | 煤的干馏是化学变化,可从得到的煤焦油中提取苯,甲苯等重要的化工原料 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com