
常温下,将0.20mol/LH2X溶液与0.20mol/LNaOH溶液等体积混合,所得溶液pH=3.6,继续滴加NaOH溶液至pH=4.0时,溶液中部分粒子浓度(Na+、H2X、HX-、X2-)如下图所示。下列说法错误的是( )
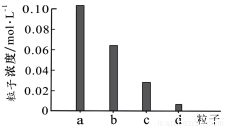
A.图中a代表Na+,d代表H2X分子
B.H2X为二元弱酸,HX-的电离程度大子水解程度
C.混合溶液pH= 3.6时:c(H+)+c(H2X)=c(x2-)+c(OH-)
D.继续滴加NaOH溶液至pH= 7.0时:c(Na+) >c(HX-)+2c(X2-)
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案科目:高中化学 来源:2016-2017年黑龙江佳木斯一中高一上9.10周练化学卷(解析版) 题型:选择题
在相同的温度和压强下,二氧化碳和笑气(化学式为N2O)的体积相同,则下列一定相同的是( )
(1)分子数 (2)原子数 (3)密度 (4)质量 (5)物质的量
A.只有(1)(5)
B.只有(1)(2)(4)(5)
C.只有(2)(3)(4)(5)
D.(1)(2)(3)(4)(5)
查看答案和解析>>
科目:高中化学 来源:2017届湖南省高三上学期9月月考化学试卷(解析版) 题型:选择题
在一种酸性溶液中,可能存在NO3-、I-、Cl-、Fe3+中的一种或几种离子,向该溶液中加入溴水,溴单质被还原,则以下推测中不正确的是
A.一定有碘离子 B.可能含铁离子 C.可能有氯离子 D.不含硝酸根离子
查看答案和解析>>
科目:高中化学 来源:2017届河南省高三上学期第一次月考化学试卷(解析版) 题型:实验题
下列实验步骤是兴趣小组对某混合样品含量的测定,样品成分为FeO、FeS2、SiO2、及其它杂质,杂质不与酸碱反应,受热稳定。(步骤中所加试剂均为足量)
①称量mg样品灼烧。装置如下:
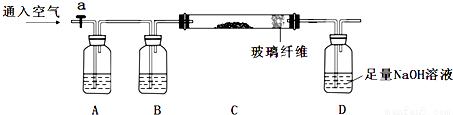
②D瓶溶液
 固体(ag)
固体(ag)
③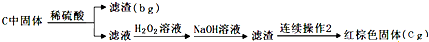
请回答下列问题:
(1)连接好仪器后,如何检查整套装置的气密性_______________。
(2)A瓶内所盛试剂是__________溶液。灼烧完成后熄灭酒精灯,若立即停止通空气,可能对实验的影响是(写两点) _________________________。
(3)步骤②中加入双氧水的离子方程式为____________________。若此步骤不加入双氧水对测定硫元素含量的影响是_____________(填“偏高”、“偏低”或“无影响”)。
(4)连续操作1为_________、洗涤、_________、称量;连续操作2为洗涤、_________、称量。
(5)从步骤③的bg滤渣入手,可测定SiO2的含量,下面各组试剂中不适合测定的是___________。
A.NaOH溶液 、稀硫酸 B.Ba(OH)2溶液、盐酸 C.氨水、稀硫酸 D.NaOH溶液、盐酸
(6)求样品中FeO的质量分数(列出算式即可)____________________。
查看答案和解析>>
科目:高中化学 来源:2017届河南省高三上学期第一次月考化学试卷(解析版) 题型:选择题
如图所示的装置,C、D、E、F、X、Y都是惰性电极,将电源接通后,向(乙)中滴入酚酞溶液,在F极附近显红色,则以下说法正确的是( )

A.电源B极是正极
B.(甲)、(乙)装置的C、D、E、F电极均有单质生成,其物质的量比为1:2:2:2
C.欲用(丙)装置给铜镀银,H应该是Ag,电镀液是AgNO3溶液
D.装置(丁)中X极附近红褐色不变
查看答案和解析>>
科目:高中化学 来源:2017届河南省高三上学期第一次月考化学试卷(解析版) 题型:选择题
在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若两容器的温度和压强均相同,且甲的密度大于乙的密度,则下列说法正确的是( )
A.甲的分子数比乙的分子数多
B.甲的物质的量比乙的物质的量小
C.甲的气体摩尔体积比乙的气体摩尔体积小
D.甲的相对分子质量比乙的相对分子质量小
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上学期9月月考化学试卷(解析版) 题型:选择题
下列有关离子方程式,正确的是
A.稀硝酸和过量的铁屑反应:Fe+4H++NO3-=Fe3++NO↑+2H2O
B.NH4HCO3溶液与足量的NaOH溶液混合加热:NH4++HCO3-+2OH- NH3↑+CO32-+2H2O
NH3↑+CO32-+2H2O
C.碳酸氢钠溶液水解的离子方程式:HCO3-+H2O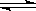 CO32-+H3O+
CO32-+H3O+
D.Fe(OH)3溶于氢碘酸中:Fe(OH)3+3H+=Fe3++3H2O
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高二上第一次月考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.增大反应物浓度,可增大活化分子的百分数,从而使有效碰撞次数增大
B.有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大
C.升高温度能使化学反应速率增大,主要原因是增加了反应物分子中活化分子的百分数
D.催化剂不影响反应活化能但能增大单位体积内活化分子百分数,从而增大反应速率
查看答案和解析>>
科目:高中化学 来源:2017届贵州省、贵阳一中高三上月考化学试卷(解析版) 题型:推断题
I、请根据如下图所示转化关系回答有关问题。A和B均为钠盐的水溶液,A呈中性,B呈碱性并具有强氧化性。
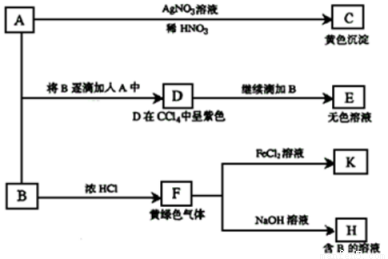
(1)写出A、B的化学式:A ,B 。
(2)依次写出A→D和D→E(E中含有某+5价元素的含氧酸根离子)的离子方程式: , 。
(3)写出将SO2气体通入K溶液中发生反应的离子方程式: 。
II、(1)将0.4gNaOH和1.06gNa2CO3混合并配成溶液,向溶液中滴加0.1mol·L-1稀盐酸。在如下图所示坐标系中画出能正确表示加入盐酸的体积和生成CO2的物质的量的关系图像。
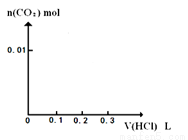
(2)将18.4gNaOH和NaHCO3固体混合物,在密闭容器中加热到约250℃,经充分反应后排出气体,冷却,称得剩余固体质量为16.6g。试计算混合物中NaOH的质量分数。(请写出计算过程)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com