
| A、白磷和硫的熔化 |
| B、冰和干冰的熔化 |
| C、食盐与蔗糖的熔化 |
| D、氧化镁和金属镁的熔化 |


科目:高中化学 来源: 题型:
A、HClO 电子式: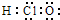 | ||
B、CH4 比例模型: | ||
| C、乙炔结构简式:HC≡CH | ||
D、质子数55,中子数82的原子
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Br2+2HI═I2+2HBr |
| B、2FeCl2+Cl2═2FeCl3 |
| C、2FeCl2+2HCl+I2═2FeCl3+2HI |
| D、Cl2通入到NaBr和NaI的混合溶液中:I-先被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、KNO3、NaOH、HCl |
| B、Ca(OH)2、HCl、NaCl |
| C、H2SO4、Na2CO3、Ba(OH)2 |
| D、HNO3、KOH、CuSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 酸 | 碱 | 盐 | 氧化物 | |
| A | H2SO4 | Na2CO3 | NaCl | SiO2 |
| B | HBr | NaOH | Na2CO3 | CaO |
| C | CO2 | NH3?H2O | NaHCO3 | CuO |
| D | CH3COOH | KOH | KCl | HClO3 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,3.2 g O2和O3的混合气中氧原子数为0.2NA |
| B、1L2mol?L-1 K2S溶液中S2-和HS-的总数为2NA |
| C、标准状况下,22.4L的CCl4中含有的CCl4分子数为NA |
| D、50mL18mol?L-1浓硫酸与足量铜微热反应,转移的电子数为1.8NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
 醇脱水反应在不同温度条件下得到的产物组成不同.下表是常压、某催化剂存在条件下,分别以等量乙醇在不同温度下进行脱水实验获得的数据,每次实验反应时间均相同.
醇脱水反应在不同温度条件下得到的产物组成不同.下表是常压、某催化剂存在条件下,分别以等量乙醇在不同温度下进行脱水实验获得的数据,每次实验反应时间均相同.| 温度(℃) | 乙醇转化率(%) | 有机产物含量(体积分数) | |
| 乙烯(%) | 乙醚(%) | ||
| 125 | 20 | 8.7 | 90.2 |
| 150 | 68 | 16.7 | 82.2 |
| 175 | 88 | 32.3 | 66.8 |
| 200 | 90 | 86.9 | 12.1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com