
【题目】短周期元索M、N、X、Y、Z的原子序数依次增大,它们组成的单质或化合物存在如下转化关系。甲、丁为二元化合物(两种元素形成的化合物),乙、戊为单质,丙、己为三元化合物。已知25℃时,0.1mol/L的甲、丙两溶液的pH分别为l、13 ,丁、己两溶液混合时产生白色沉淀。下列推断正确的是

A. M分别与N、X、Z形成的简单化合物中,M与N形成的化合物熔点最高
B. 原子半径:Z>Y>X>M>N
C. X、Y、Z的最高价氧化物对应的水化物能相互反应
D. Z的阴离子结合质子的能力比N的阴离子强
【答案】C
【解析】25℃时,0.1 molL-1甲溶液的pH=1,说明甲为一元强酸,甲为二元化合物,短周期中只有HCl满足;0.1molL-1丙溶液的pH=13,说明丙为一元强碱,短周期元素中只有Na对应的NaOH为强碱,所以M为H元素;乙为单质,能够与强酸甲、强碱丙反应生成单质戊,则戊只能为氢气,乙为金属Al;结合M,N,X,Y,Z的原子序数依次增大可知为H、O、Na、Al、Cl元素,则A. M分别与N、X、Z形成的简单化合物分别是H2O、NaH、HCl,NaH是离子化合物,熔点最高,A错误;B. 同周期自左向右原子半径逐渐减小,同主族自上而下原子半径逐渐增大,则原子半径:Na>Al>Cl>O>H,B错误;C. X、Y、Z的最高价氧化物对应的水化物分别是氢氧化钠、氢氧化铝和高氯酸,三者能相互反应,C正确;D. 盐酸是强酸,因此氯离子结合氢离子的能力比O的阴离子弱,D错误,答案选C。


科目:高中化学 来源: 题型:
【题目】有人设计了一套实验分馏原油的五个步骤:

①将仪器a固定在铁架台上,在仪器a上塞好带温度计的橡皮塞.
②连接好冷凝管.把冷凝管固定在铁架台上,将冷凝管进水口的橡皮管的一端和水龙头连接,出水口相接的橡皮管的另一端放在水槽中.
③把酒精灯放在铁架台上,调整铁圈的高度,放好石棉网.
④向仪器a中放入几片碎瓷片,再用漏斗向仪器a中加入原油,塞好带温度计的橡皮塞,把连接器连接在冷凝器的末端,并伸入接收装置(如锥形瓶)中.
⑤检查气密性(利用给固定装置微热的方法).请完成以下问题:
(1)上述实验正确的操作顺序是:______(填序号).
(2)仪器a的名称为:______.
(3)冷凝管里水流的方向为____进____出.(填f或g,注:上为f下为g).
(4)分馏原油是利用了原油中各组分的______不同而达到分离的目的.
(5)仪器a中放几片碎瓷片的目的是______.
(6)在实际工业生产中,除石油的分馏,人类利用煤炭的历史也很悠久,从煤焦油中能分离得到了一种重要化工原料“苯”,请写出该物质与浓硝酸反应的化学方程式:____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修5]有机化学基础:有机物丙(C13H18O2)是一种香料.其可由甲和乙在浓硫酸催化作用和加热条件下合成:

已知以下信息.:
①甲的相对分子质量为88,它的核磁共振氢谱显示有3组峰;
②乙为香醇的同系物.香醇的结构简式为:
③![]()
回答下列问题:
(1)A的名称为____________。
(2)B的分子式为______________。
(3)C与新制碱性Cu(OH)2反应的化学方程式为____________。
(4)丙中有两个甲基.在一定条件下,1 mol D可以和2 mol H2反应生成乙.D可以发生银镜反应.则D 的结构简式为____________。
(5)甲与乙反应的化学方程式为______________,该反应类型为_________________:
(6)甲的同分异构体中含有“COO”结构的共有_____________种(不包含甲),其中核磁共振氢谱为3组 峰。且峰面积之比为6:1:1的为______________(写结构简式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若甲烷与氯气以物质的量之比1:3混合,在光照下得到的产物:(1)CH3Cl,(2)CH2Cl2,(3)CHCl3,(4)CCl4,其中正确的是( )
A只有(1)B(1)(2)(3)(4)的混合物 C只有(3) D(1)(2)(3)的混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是元素周期表的一部分,针对表中的①~⑩中元素,填写下列空格:
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
二 | ① | ② | ③ | |||||
三 | ⑥ | ④ | ⑤ | ⑦ | ⑩ | ⑧ | ⑨ |
⑴在这10种元素中,非金属性最强的元素是_____ (填“元素符号”);金属性最强的元素是_____(填“元素符号”);化学性质最不活泼的元素是_______(填“元素符号”);元素②简单离子的结构示意图为___________________。
⑵元素①与②中,原子半径较大的是________(填元素符号)。
⑶元素②与⑦的气态氢化物分别为__________和__________ (填化学式),两者的热稳定性大小为:前者_____后者。(填“>”、“<”或“=”)。
⑷元素④与⑧的最高价氧化物的水化物分别为______和______(填“化学式”),
两者反应的离子方程式为__________________________________。
⑸元素⑤的氧化物与盐酸反应的离子方程式为: _______________________。
⑹元素⑧的单质与元素⑩的氢化物反应的化学方程式为:__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)用甲烷—空气碱性(KOH溶液)燃料电池作电源,电解CuCl2溶液。装置如图所示:
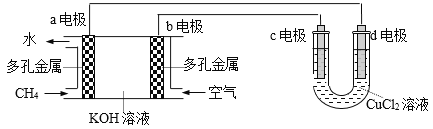
①a电极名称为_______。
②c电极的电极反应式为_________________。
③假设CuCl2溶液足量,当某电极上析出3.2 g 金属Cu时,理论上燃料电池消耗的空气在标准状况下的体积是_______L(空气中O2体积分数约为20%)。
(2)在一定条件下,恒温恒容密闭容器中进行可逆反应:N2+3H2![]() 2NH3。
2NH3。
①试判断下列情况能说明该反应已经达到化学平衡状态的是________________(填字母序号)。
a.单位时间内生成n mol N2同时生成3n mol H2
b.H2的生成速率等于NH3的生成速率
c.一个N≡N键断裂的同时,有三个H—H键形成
d.容器中N2、H2、NH3的浓度之比为1∶3∶2
e.反应物浓度等于生成物浓度
f.混合气体的总物质的量不变
②298 K时,若已知生成标准状况下2.24 L NH3时放出热量为4.62 kJ。写出合成氨反应的热化学方程式_____________________。在该温度下,取1 mol N2和3 mol H2放在一密闭容器中,在催化剂存在时进行反应。测得反应放出的热量总小于92.4 kJ,其原因是_______________________。
(3)某课外活动小组用下图装置进行实验,试回答:

①若开始时K接M,则铁极上的电极反应式为______,石墨极上的电极反应式为________。
②若开始时K接N,则石墨极上的电极反应式为______,电解的总化学方程式为_______。
(4)常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示,反应过程中有红棕色气体产生。
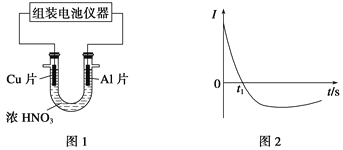
0~t1时,原电池的负极是Al片,此时,正极的电极反应式是________,溶液中的H+向_____极移动。t1时,原电池中电子流动方向发生改变,其原因是____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com