
Na、Cu、O、Si、S、Cl是常见的六种元素。
(1)Na位于 元素周期表第 周期第 族;S的基态原子核外有 个未成对电子;Si的基态原子核外电子排布式为 。
元素周期表第 周期第 族;S的基态原子核外有 个未成对电子;Si的基态原子核外电子排布式为 。
(2)用“>”或“<”填空:
| 第一电离能 | 离子半径 | 熔点 | 酸性 |
| Si S | O2- Na+ | NaCl Si | H2SO4 HClO4 |
(3)CuCl(s)与O2反应生成CuCl2(s)和一种黑色固体。在25 ℃、101KPa下,已知该反应每消耗1 m ol CuCl2(s),放热44.4KJ,该反应的热化学方程式是 。
ol CuCl2(s),放热44.4KJ,该反应的热化学方程式是 。
(4)ClO2是常用于水的净化,工业上可用Cl2氧化NaClO2溶液制取ClO2。写出该反应的离子方程式,并标出电子转移的方向和数目 。
科目:高中化学 来源: 题型:
(1)[2012·新课标全国卷,36(3)]粗铜的电解精炼如图所示。在粗铜的电解过程中,粗铜板应是图中电极________(填图中的字母);在电极d上发生的电极反应式为__________;若粗铜中还含有Au、Ag、Fe,它们在电解槽中的存在形式和位置为____________。

(2)(2012·海南,16)新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2 ,电解质为KOH溶液。某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液电解实验,如图所示。
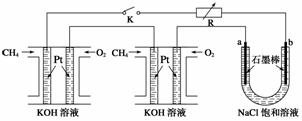
回答下列问题:
①甲烷燃料电池正极、负极的电极反应分别为________________________________、
________________________________________________________________________。
②闭合K开关后,a、b电极上均有气体产生,其中b电极上得到的是__________,电解氯化钠溶液的总反应方程式为
________________________________________________________________________。
③若每个电池甲烷通入量为1 L(标准状况),且反应完全,则理论上通过电解池的电量为__________(法拉第常数F=9.65×104 C · mol-1列式计算),最多能产生的氯气体积为________L(标准状况)。
查看答案和解析>>
科目:高中化学 来源: 题型:
W、X、Y、Z均是短周期元素,X、Y处于同一周期,X、Z的最低价离子分别为X2-和Z- ,Y+和Z-离子具有相同的电子层结构。下列说法正确的是( )
A.原子最外层电子数:X>Y>Z B.单质沸点:X>Y>Z
C.离子半径:X2->Y+>Z- D.原子序数:X>Y>Z
查看答案和解析>>
科目:高中化学 来源: 题型:
元素周期表中第VIIA族元素的单质及其化合物的用途广泛。
(1)与氯元素同族的短周期元素的原子结构示意图为 。
(2)能作为氯、溴、碘元素非金属性(原子得电子能力)递变规律的判断依据是 (填序号)。
a.Cl2、Br2、I2的熔点 b. Cl2、Br2、I2的氧化性
c.HCl、HBr、HI的热稳定性 d. HCl、HBr、HI的酸性
(3)工业上,通过如下转化可制得KClO3晶体:
NaCl溶液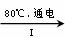 NaClO3溶液
NaClO3溶液 KClO3晶体
KClO3晶体
①完成I中反应的总化学方程式:□NaCl+□H2O=□Na ClO3+□
ClO3+□ 。
。
②II中转化的基本反应类型是  ,该反应过程能析出KClO3晶体而无其它晶体析出的原因是 。
,该反应过程能析出KClO3晶体而无其它晶体析出的原因是 。
(4)一定条件,在水溶液中1 mol Cl-、ClO-(x=1,2,3,4)的能量(KJ)相对大小如右图所示。

①D是  (填离子符号)。
(填离子符号)。
②B→A+C反应的热化学方程式为 (用离子符号表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
为实现下列 实验目的,依据下表提供的主要仪器,所用试剂合理的是
实验目的,依据下表提供的主要仪器,所用试剂合理的是
| 选项 | 实验目的 | 主要 | 试剂 |
| A | 分离Br2和CCl4混合物 | 分液漏斗、烧杯 | Br2和CCl4混合物、蒸馏水 |
| B | 鉴别葡萄糖和蔗糖 | 试管、烧杯、酒精灯 | 葡萄糖溶液、蔗糖溶液、银氨溶液 |
| C | 实验室制取H2 | 试管、带导管的橡皮塞 | 锌粒、稀HNO3 |
| D | 测定NaOH溶液浓度 | 滴定管、锥形瓶、烧杯 | NaOH溶液,0.1000mol/L盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列措施对增大反应速率明显有效的是( )
A、Na与水反应时增大水的用量 B、Fe与稀硫酸反应制取氢气时,改用浓硫酸
C、在H2SO4与Na2CO3两溶液反应时,增大压强 D、反应N2+3H2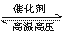 2NH3恒容增加氮气
2NH3恒容增加氮气
查看答案和解析>>
科目:高中化学 来源: 题型:
有A、B、C、D、E、F六种元素,期中A、B、C、D、E为短周期元素, 且原子序数依次增大。已知A和B具有相同的电子层数, 且A的L层电子数是K层电子数的两倍; C单质燃烧时呈现黄色火焰, C单质在高温下与B单质充分反应, 可以得到与D单质颜色相同的淡黄色固态化合物; E元素的最低负价为负一价;F元素位于周期表中第四周期,它的氧化物中有一种常做涂料和红色油漆。试根据以上叙述回答:
(1)写出下列元素的名称: A ________, D ___________。
(2)写出B元素在周期表中的位置 。
(3)用电子式表示化合物 C2D 的形成过程 ___________________________。
(4)A与B形成的化合物均对环境能产生影响,请你写出一例 。
(5)写出B单质与C单质反应生成淡黄色化合物M的化学方程式 ;写出一例M的用途_______________。
(6)如何检验FE2溶液中的金属阳离子(答操作、现象及结论)___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com