
| A. | 涂改液危害人体健康、污染环境 | |
| B. | 中学生最好不用或慎用涂改液 | |
| C. | 苯的同系物和卤代烃皆可溶于水 | |
| D. | 苯的同系物和卤代烃是涂改液中的溶剂 |
分析 A.涂改液被吸入人体或粘在皮肤上,将引起慢性中毒,同时污染环境;
B.涂改液对人体有害;
C.一般情况下,苯的同系物和卤代烃都不溶于水;
D.苯的同系物和卤代烃均为常见的有机溶剂.
解答 解:A.涂改液被吸入人体或粘在皮肤上,将引起慢性中毒,同时污染环境,应减少使用,故A正确;
B.涂改液对人体有害,中学生最好不用或慎用涂改液,故B正确;
C.烃基、-X均为憎水剂,苯的同系物和卤代烃都不溶于水,故C错误;
D.苯的同系物和卤代烃均为常见的有机溶剂,则苯的同系物和卤代烃是涂改液中的溶剂,故D正确;
故选C.
点评 本题考查有机物的结构与性质,为高频考点,把握有机物的性质、性质与用途为解答的关键,侧重分析与应用能力的考查,注意化学与生活的联系,题目难度不大.


科目:高中化学 来源: 题型:实验题
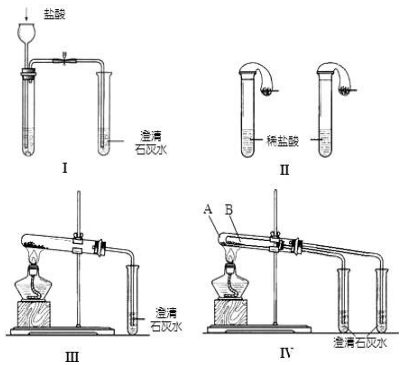
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若a≥2b,发生的反应化学方程式为:2C2H2+O2═4C+2H2O | |
| B. | 若($\frac{2}{5}$)b<a<($\frac{2}{3}$)b,燃烧后在密闭容器中加入含amolCa(OH)2的石灰水,发生反应的离子方程式为:OH-+CO2═HCO3- | |
| C. | 若a<($\frac{2}{5}$)b,燃烧过程中转移的电子的物质的量为10amol | |
| D. | 若a=($\frac{1}{2}$)b,燃烧产物既有CO2又有CO,且n(CO2):n(CO)=1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu2+、Na+、SO42-、Cl- | B. | Ba2+、Na+、OH-、SO42- | ||
| C. | OH-、HCO3-、Mg2+、Na+ | D. | K+、Na+、OH-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 四种元素均为非金属元素 | |
| B. | W与X、Y形成的最简单分子的沸点:X>Y | |
| C. | Y、Z形成的化合物中只含离子键 | |
| D. | W、Y、Z形成的化合物的电子式为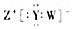 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铍的原子失电子能力比镁弱 | B. | 砹(At)的氢化物不稳定 | ||
| C. | 硒的原子半径比硫小 | D. | Sr(OH)2 比Ca(OH)2 碱性强 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金刚石和石墨互为同素异形体,熔点和硬度都很高 | |
| B. | 氕、氘、氚是氢元素的三种核素,质子数都是1 | |
| C. | 乙醇和二甲醚(CH3-O-CH3)互为同系物 | |
| D. | C4H10的一氯代物只有一种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe和醋酸反应:Fe+2H+═Fe2++H2↑ | |
| B. | 大理石和稀盐酸反应:CO32-+2H+═CO2↑+H2O | |
| C. | FeCl2溶液与Cl2的反应:2Fe2++Cl2═2Fe3++2Cl- | |
| D. | Cl2与H2O反应:Cl2+H2O═2H++Cl-+ClO- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com